Как избавиться от старых митохондрий
Некоторые нейроны прибегают к помощи астроцитов
В науке широко признано, что клетки сами разрушают и перерабатывают свои старые или поврежденные органеллы, но недавно ученые Школы медицины Калифорнийского университета в Сан-Диего (University of California, San Diego School of Medicine), Школы медицины Университета Джонса Хопкинса (Johns Hopkins University School of Medicine) и Института Кеннеди Кригера (Kennedy Krieger Institute) подвергли правильность этого положения обоснованному сомнению, продемонстрировав, что некоторые нейроны передают функцию утилизации ненужных им митохондрий – крошечных внутриклеточных энергетических станций – клеткам глии, известным как астроциты.
Подтверждающие их выводы данные, опубликованные в раннем онлайн издании PNAS (Davis et al., Transcellular degradation of axonal mitochondria), предполагают необходимость пересмотра некоторых из основ биологии. Но они имеют и практическое значение, углубляя понимание многих нейродегенеративных заболеваний и метаболических расстройств и открывая путь к усовершенствованию методов их лечения.
«Это подвергает сомнению общепринятый постулат, что клетки обязательно сами разрушают свои органеллы. Мы пока не знаем, насколько этот процесс генерализован, если рассматривать мозг в целом, но наша работа предполагает его вероятную широкую распространенность», – говорит один из ведущих соавторов исследования Марк Эллисман (Mark Ellisman), PhD, заслуженный профессор неврологии, директор Национального научно-исследовательского центра микроскопии и визуализации (National Center for Microscopy and Imaging Research) UC San Diego.
«Открытие стандартного процесса передачи мусора от нейронов к глии, по всей вероятности, будет очень важно для понимания возрастного снижения функций головного мозга и нейродегенеративных или метаболических заболеваний», – комментирует результаты исследования другой его ведущий соавтор Николас Марш-Армстронг (Nicholas Marsh-Armstrong), PhD, невролог из Университета Джонса Хопкинса и Института Кеннеди Кригера. «Мы ожидаем, что оно окажет значительное влияние и на другие области биомедицины».
Ученые сосредоточили свое внимание на аксонах ганглионарных клеток сетчатки – нейронов, передающих визуальную информацию от глаза к головному мозгу. Стимулом к проведению этого исследования стали наблюдения, сделанные доктором Марш-Армстронгом в ходе изучения мышиной модели глаукомы, о том, что белковые продукты из сетчатки накапливаются в головке зрительного нерва непосредственно за глазом.
Реконструкция данных электронной микроскопии, показывающая часть ганглиозной клетки сетчатки (синяя) в головке зрительного нерва нормальной здоровой мыши. Две ее выпуклости заполнены митохондриями (красные). Ученые считают, что это – один из этапов процесса выведения митохондрий для дальнейшего их разрушения соседними астроцитами. (Фото: Keun-Young Kim/PNAS)
Используя передовые методы микроскопии и молекулярные методики, разработанные в лабораториях Эллисмана и Марш-Армстронга, исследователи установили, что поврежденные митохондрии ганглионарных клеток сетчатки собираются у головки оптического нерва – там, где аксоны ганглионарных клеток выходят из глаза, образуя идущий к мозгу зрительный нерв. Эти митохондрии поглощаются и разрушаются соседними астроцитами – самыми распространенных глиальными клетками нервной системы позвоночных и единственными клетками, связывающими нейроны головного мозга с кровью.
Зрительный нерв и сетчатка мыши, ответственные за передачу информации от глаза к головному мозгу. Ткань окрашена флуоресцентными веществами, показывающими распределение астроцитов (желтые), аксонов ганглионарных клеток сетчатки (фиолетовые), миелина (зеленый) и ядер клеток (голубой). Аксоны ганглионарных клеток сетчатки передают митохондрии близлежащим астроцитам в головке зрительного нерва позади сетчатки. Астроциты разрушают эти митохондрии в процессе, названном трансмитофагией. (Фото: Mark Ellisman, NCMIR, UC San Diego)
Это открытие опровергает общепризнанную аксиому, что все клетки сами изолируют, разрушают и удаляют поврежденные молекулы и органеллы – процесс, известный как аутофагия (в переводе с греческого «самопоедание»). Если в этот процесс вовлечены митохондрии, он называется митофагией. Процесс, описанный Марш-Армстронгом, Эллисманом и их коллегами, назван трансмитофагией (transmitophagy).
Однако многие вопросы, связанные с этим удивительным открытием, пока остаются без ответа. Например, происходят ли митохондрии, перемещаемые к головке зрительного нерва, только из популяции, находящейся в длинных проводящих нервных волокнах, идущих от глаза к мозгу, или какие-то митохондрий активно транспортируются из самой сетчатки?
По мнению доктора Эллисмана, результаты этого исследования углубят понимание – и, возможно, в конечном итоге, усовершенствуют лечение – целого ряда заболеваний.
«Митохондрии играют важную роль в здоровье аксонов, совершенно необходимых для взаимодействия нейронов и передачи информации. Дальнейшее изучения того, что происходит в процессе трансмитофагии и вносят ли нарушения в этом явлении вклад в развитие нейрональных дисфункций или заболеваний, должно стать приоритетным направлением исследований», – считает ученый.
Значение результатов этого исследования выходит далеко за рамки зрительного нерва, так как накопление внутри клеток «мусора» вызывает нейродегенеративные заболевания, такие как болезнь Паркинсона, болезнь Альцгеймера и боковой амиотрофический склероз, говорит доктор Марш-Армстронг. «Показав существование этого альтернативного вида утилизации, мы открыли другим путь к изучению того, могут ли подобные процессы происходить с другими типами клеток или с другими, помимо митохондрий, клеточными компонентами».
Источник
АТФ — главный энергетический спонсор клетки. Или где взять энергию? Митохондриальные дисфункции.
Сегодня внедряемся в научные изыскания. Статья будет сложной для прочтения. Я максимально упрощала материал, но проще — некуда. На написание меня как всегда «вдохновила» всеобщая бесконечная жалоба — «слабость, ничего не помогает, ваших капельниц, таблеток хватило на 2 недели. «. Сегодня рассмотрим самый сложный случай дефицита Энергии — дисфункция Митохондрий. Это еще малоизученная и сложная часть медицинской науки. Дисфункция митохондрий может быть врожденная и в нашем (рассматриваемом случае) — приобретенная.
Энергия в нашем организме представлена в следующем виде — молекула АТФ.
АТФ-аденозинтрифосфат, является основным источником энергии для клеток в частности и организма в целом. Представляет собой — эфир аденозина (пурин). Кроме того, является источником синтеза нуклеиновых кислот, для образования структуры ДНК!(наш генетический код)и посредником передачи в клетку гормонально сигнала! Вывод: нехватка АТФ — чревата извращение/недостатком гормонального ответа и не только. АТФ образуется в митохондриях (это маленькие структурные компоненты любой клетки, митохондрия имеет собственную ДНК!, как и ядро клетки. это высокоорганизованная структура ). Вот почему заболевания с нарушением синтеза АТФ — называются митохондриальные дисфункции.
В сутки в организме образуется 40 кг АТФ. Органы с максимальной выработкой АТФ: мозг 22%, печень 22%, мышцы 22 %, сердце 9%, жировая ткань всего — 4%, заметьте — ЩЖ с в этот перечень даже не вошла. Мозг и печень лидеры !
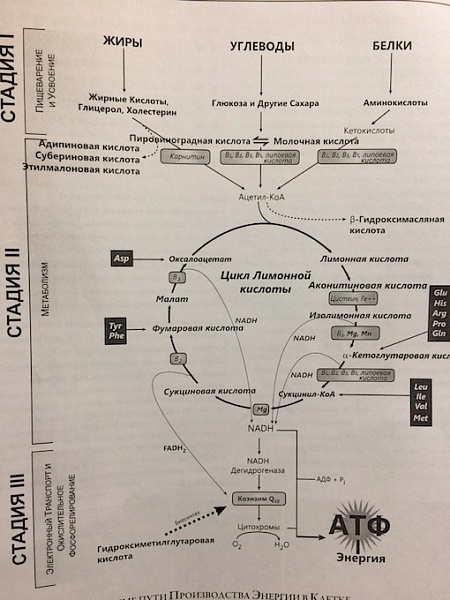
Теперь о самом процессе образования энергии. Смотрим на картинку.
Процесс образования энергии можно разделить на 3 этапа.
1 этап — это получение более простых молекул( в цикл образования энергии) из углеводов(У), жиров(Ж) и белков пищи(Б). Углеводы расщепляются до моносахаров(глюкоза,фруктоза), жиры до жирных кислот, белки до аминокислот. «Расщепление» Б,Ж,У происходит как к кислородной среде(аэробной), так и в бескислородной(анаэробной) среде. Это крайне важно! Так как из анаэробного гликолиза 1 молекулы глюкозы образуется — 2 молекулы АТФ, из аэробного (кислородного) гликолиза 1 молекулы глюкозы — образуются 36 молекул АТФ, из аэробного окисления 1 молекулы жирной кислоты — 146 молекул АТФ, ( жиры и белки в бескислородной среде вообще не расщепляются!, вывод — например, при нелеченной анемии(дефицитО2) снижение веса почти невозможно). Так, и усвоение 1 молекулы глюкозы требует 6 молекул О2, а 1 молекулы жирных кислот -23 молекулы О2. Вывод — жиры основной источник энергии, и всем нужен О2.
2 этапом — образуется из всех молекул У, Ж, Б — АцетилКоА — промежуточный метаболит. Суть этого этапа, что кол-во выработанного АцетилКоА зависит от уровня многих витаминов и микроэлементов (витамина С, группы В, цинка, меди, железа и др). Почему так важно для образования энергии — восполнение дефицита этих элементов!
3 этап — этот самый АцетилКоА поступает в 2 основных биохимических пути выработки АТФ — это цикл Кребса( лимонной кислоты) и цикл окислительного фосфорилирования ( передачи электронов, «дыхательная цепь»;), происходит образование НАД- и НАДН+. Связь между этими двумя б/х циклами — и «есть узкое горлышко», «слабое место» в образовании АТФ. И зависит от рН среды клетки — при развитии в/клеточной гипоксии = в/клеточного ацидоза и ухудшается процесс образования АТФ — организм захлебывается в избытке НАДН, а НАДН сопряжен с «утечкой кислорода из клетки»( механизм не буду расшифровывать) и образованием активных(агрессивных) форм кислорода ( свободных радикалов) — а это повреждающие агенты для клетки при образовании в избыточном количестве.
Метаболический ацидоз — это следствие первичного дефицита О2 в организме (сам ацидоз становится причиной вторичного дефицита О2-утечки кислорода). Ацидоз выражается накоплением промежуточного продукта обмена — лактата, избытком Н+(иона водорода), митохондрии «начинают задыхаться и стареть и гибнуть»! А в месте со старением митохондрий — стареет организм, вот почему так молодеют некоторые заболевания — раньше развиваются атеросклероз, б-нь Альцгеймера, сахарный диабет (да-да , это митохондриальное заболевание), рак, артериальная гипертензия, АИТ, синдром хр усталости, даже НЯК и болезнь Крона (как одна из теорий) и др.
Как цикл лимонной кислоты (цикл Кребса) , например, связан с ожирением? — активное поступления с пищей жирных кислот- приводят к истощению транспортных карнитиновых (всем известен для сравнения Карнитин для спорт -питания) систем( переносчиков жирных кислот, их и так немного) и снижения активности работы «дыхательной цепи» , снижается чувствительность тканей к инсулину- развивается многим известная инсулинорезистентость! Исход — метаболическая печалька — метаболический синдром.
Соответственно: причинами снижения синтеза АТФ прежде всего являются дефицит О2!(как бывает в больших городах, где мало зелени. загазованность — продукт сгорания бензина это не О2-а СО2 . люди не выходят из помещений, мало двигаются — «мелкие сосуды закрыты для доступа О2», причинами могут быть болезни органов дыхания и сердечно-сосудистые патологии), ацидоз = «закисление организма» (накопление лактата, избыток Н+), полидефицит витаминов и микроэлементов для улучшения усвоения Ж, Б, У. Для лечение дефицита О2 даже был придуман аппарат — в основе которого интервальная гипоксическая тренировка. Это новая эра в лечении многих патологий.
Как же заподозрить митохондриальные проблемы? Они сложны как для понятия, так и для диагностики.
Из «простых анализов», которые можно набрать любой лаборатории — снижение рН крови, О2, повышение: лактата, СРБ, фибриногена, холестерина, ЛПНП, триглицеридов, гомоцистеина, мочевой кислоты, (клинически — повышение Ад, учащение ЧСС в покое, одышка в покое), снижение ферритина, из редких — снижение глутатиона, витаминов крови, снижение Q10, нарушение в системе антиоксидантов (по крови).
Из более редких , но все же доступных анализов (более специфических) — органические кислоты мочи ( благодаря этому анализу можно определить примерно на каком уровне идет нарушение и чем его скорректировать).
Если патология так сложно выявляемая — «как это лечить?»,- спросите вы
Прежде всего меняем образ жизни — улучшаем доставку О2!, бросаем курить! чаще дышим в парке и не только.. Лечим и приводим в ремиссию хронические дыхательные заболевания , восполняем дефицит витаминов и минералов!, добавляем антиоксиданты, сосудистые препараты(!) очень важно улучшить коровок(слабость всегда сопровождается рассеянностью, снижением памяти и внимания, — правильно, максимальная сосудистая сеть в головном мозге!!), реже добавляем «энергетики» — янтарная кислота, Q10, карнитин, НАДН и др. Я не говорю здесь про врожденные митохондриальные дисфункции — это следствие генетической поломки,а мы говорим сейчас больше о приобретенных причинах. Будем ждать новых научных материалов по этой теме.
Источник
Продление жизни: отключите белки трансляционного контроля митохондрий
Как митохондрии управляют старением
Кирилл Стасевич, Компьюлента
Митохондрии влияют на процессы старения не только через окислительный стресс, источником и ликвидатором которого она является. Подавление активности белков, обслуживающих синтез в митохондриях, приводит к увеличению жизни клетки, независимо от её чувствительности к окислительному стрессу.
Митохондрия клетки кишечного эпителия.
На внутренних складках мембраны протекают окислительные реакции клеточного дыхания.
(Фото professors P. Motta & T. Naguro.)
Митохондрии давно подозревались в причастности к процессам старения. Эти клеточные органеллы обеспечивают клетку энергией, в прямом смысле сжигая внутри себя разнообразное топливо: питательные вещества окисляются в митохондриях кислородом, и после целой череды биохимических реакций получается высокоэнергетическая молекула АТФ, которую клетка может использовать для своих целей. Ну а поскольку в добыче энергии задействован кислород, попутно происходит накопление вредных побочных продуктов – свободных радикалов. Они довольно агрессивны и могут нарушать химические связи в самых разных биомолекулах, в том числе в белках и ДНК.
У митохондрии есть инструменты для гашения этих опасных окислителей, но со временем радикалов становится больше, и защитные системы клетки перестают справляться с ними. Окислительный стресс выходит из-под контроля. Вот так и получается, что энергостанции-митохондрии, в силу вредности профессии, играют довольно серьёзную роль в дряхлении клетки и организма.
Учёные из Гётеборгского университета (Швеция) обнаружили, что выключение некоторых митохондриальных белков замедляет процесс старения. Вроде бы ничего удивительного, но эти белки, как оказалось, не имеют никакого отношения к энергетике и окислительным процессам. Речь идёт о белках внутреннего хозяйства, называемых белками трансляционного контроля митохондрий (МТС – mitochondrial translational control) и необходимых для нормального биосинтеза в этих органеллах. (Митохондрии, к слову, замечательны ещё и тем, что у них собственный, независимый от остальной клетки геном и собственный же белоксинтезирующий аппарат; в этом смысле митохондрии представляют собой что-то вроде государства в государстве.)
Но вот эти МТС-белки, как оказалось, имеют полномочия, выходящие за пределы митохондрий: они влияют на стабильность генома клетки, упаковку хроматина и способность клетки избавляться от повреждённых и опасных белков. Митохондриальные белки обнаружили себя в тесном сотрудничестве с некоторыми из сигнальных молекул клетки, которые управляют активностью других белков, ответственных за состояние хромосом и уборку белкового «мусора» – испорченных и повреждённых молекул. Исследователи экспериментально подавляли синтез ряда белков из МТС-группы, и в результате наблюдали «засыпание» значительной части клеточного генома (ДНК в хромосомах оказывалась плотно упакована и закрыта от чтения), увеличение срока жизни клеточных белков и активизацию «систем уборки»; клетка как бы сбавляла рабочие обороты и начинала лучше следить за собой.
Итог: при выключенных МТС-белках клетки жили дольше. И что более важно – на продление жизни таким способом не оказывала влияние чувствительность клеток к свободным радикалам. Так, клетки дрожжей с выключенными МТС-белками сохраняли жизнеспособность одинаково долго даже тогда, когда у них искусственно портили ферменты, отвечающие за борьбу с окислительным стрессом.
Полностью результаты исследований, посвящённых роли митохондрий в старении, опубликованы в журнале Molecular Cell (Caballero et al., Absence of Mitochondrial Translation Control Proteins Extends Life Span by Activating Sirtuin-Dependent Silencing).
С узкоспециальной точки зрения эксперименты шведских учёных объясняют несколько странных фактов, которые уже наблюдались, – когда нарушения в функционировании митохондрий приводили к увеличению жизни у грибов, дрозофил и круглых червей. Считалось, что всякие погрешности в работе этих органелл ведут лишь к усилению неконтролируемых окислительных процессов и, следовательно, к ускорению старения. Теперь можно с уверенностью сказать, что всевозможные антиоксиданты не молодильные яблоки, не панацея от смерти: на старение в обход окислительных процессов влияют те же митохондрии.
Впрочем, сами исследователи намерены заставить митохондриальные белки поработать на продление жизни: раз уж они влияют на стабильность биомолекул в клетке, нельзя ли с их помощью воспрепятствовать развитию таких заболеваний, как рак или болезнь Альцгеймера, которые как раз связаны с расшатанностью генома и нарушениями в синтезе и упаковке белков.
Источник