- Как вылечить синдром Кушинга?
- Классификация синдрома Кушинга
- Этиология синдрома Иценко-Кушинга
- Патогенез заболевания
- Синдром Иценко-Кушинга: клинические проявления
- Особенности течения медицинской проблемы у беременных
- Особенности синдрома Кушинга у детей
- Осложнения синдрома Кушинга
- Диагностика синдрома Кушинга
- Лечение синдрома Иценко-Кушинга
- Как вылечить синдром Кушинга?
- Операции при синдроме Кушинга
- Контроль излеченности
- Профилактика
- Советы и рекомендации
- Синдром Кушинга: как поставить диагноз
- В каких случаях врач общей практики должен заподозрить синдром Кушинга? Как подтвердить диагноз? Нужно ли отменять короткие курсы экзогенных кортикостероидов постепенно?
- Таблица 1. Симптомы синдрома Кушинга (в порядке частоты встречаемости)
- Случай из практики
Как вылечить синдром Кушинга?
Синдром Кушинга — это группа клинических симптомов, возникающих в результате повышения в организме уровня глюкокортикостероидов (ГКС — гормоны, вырабатываемые корой надпочечников). Наиболее важным из них является кортизол, который влияет на метаболические изменения.
Секреция ГКС корой надпочечников регулируется гипофизом. Он производит гормон под названием адренокортикотропин (АКТГ), который стимулирует надпочечники вырабатывать кортизол. Высокий уровень кортизола подавляет выработку АКТГ, а низкий уровень увеличивает выработку этих гормонов. Гиперкортицизм возникает вследствие использования пероральных кортикостероидов или при повышенном уровне кортизола в организме.
Классификация синдрома Кушинга
Существует 2 формы синдрома Кушинга:
- АКТГ-зависимая форма. В кровь пациента попадает слишком много кортикотропина, который является гормоном гипофиза. Причина — опухоль самого гипофиза. Болезнь Кушинга может быть следствием секреции АКТГ из опухоли, которая располагается за пределами самого гипофиза, например, в щитовидной или поджелудочной железе.
- АКТГ-независимая форма. Высокий уровень кортизола в организме может быть результатом гиперплазии или опухоли надпочечников.
Этиология синдрома Иценко-Кушинга
Причины синдрома Кушинга
- Экзогенные — вызванные поступлением внешних глюкокортикостероидов. Это следствие длительного использования стероидов в терапевтических целях при многих болезнях.
- Эндогенные — кортизол вырабатывается организмом в количествах, превышающих физиологические нормы на фоне онкологии.
Среди провоцирующих факторов болезни Иценко-Кушинга встречаются инфекционные поражения мозга, травмы и длительная интоксикация. Также проявление болезни иногда связывают с половым созреванием, климаксом или родами.
Патогенез заболевания
Синдром Кушинга, признаки которого довольно специфичны, образуется при избытке кортизола. Хотя этот гормон и способствует развитию патологии, он также участвует в метаболических процессах (регулирует метаболизм глюкозы, жиров и белков).
Важным фактором в развитии и эффективном лечении заболевания является причина гормональных нарушений. Наилучший прогноз имеют пациенты, у которых опухоль гипофиза или надпочечника была удалена в результате операции. При злокачественном новообразовании по окончанию лечения пациент должен находиться под наблюдением эндокринолога и проходить регулярные осмотры. Способы предотвращения болезни пока неизвестны.
Синдром Иценко-Кушинга: клинические проявления
Симптомы синдрома Кушинга:
- повышение аппетита;
- склонность к появлению синяков и отеков;
- проблемы с цветом лица;
- широкие красные или голубоватые растяжки;
- постепенная атрофия мышц конечностей;
- подверженность частым инфекциям;
- нарушения менструального цикла у женщин, импотенция у мужчин;
- покраснение, связанное с истончением кожи и расширением сосудов;
- скопление жировой ткани вокруг живота, шеи (так называемая шея буйвола) и над ключицами.
Кроме того у больных происходит разрушение костной системы, приводящее к остеопорозу, появляются признаки воспалительных состояний слизистой желудка.
Также специфическим симптомом синдрома Кушинга является лунообразная форма лица пациента.
Особенности течения медицинской проблемы у беременных
Диагностировать болезнь Иценко-Кушинга при беременности часто бывает проблематично. Уровень общего кортизола и АКТГ в таких случаях всегда выше. Симптомом заболевания у беременных является увеличение массы тела, непропорциональное сроку беременности. Другие признаки — высокое артериальное давление и легкие синяки. При стабильном течении заболевания необходимо придерживаться симптоматического лечения, а специализированную медикаментозную терапию применять после родов.
Особенности синдрома Кушинга у детей
Дети, страдающие синдромом Иценко-Кушинга, начинают медленнее расти и быстрее набирать вес. Чтобы распознать появление симптомов болезни, рекомендуется регулярно измерять и взвешивать ребенка. Многое в патогенезе зависит от возраста и от того, секретируется ли гормон стресса непрерывно или циклически.
Внешне синдром Кушинга у детей проявляется характерной бычьей шее, округлым лицом. Также приблизительно у 50 % больных детей с синдромом Кушинга наблюдается усталость, высокое артериальное давление и растяжки.
Осложнения синдрома Кушинга
Последствия синдрома Кушинга связаны с формированием гипертонии, ИБС, диабета и язвенной болезни. Также увеличивается риск остеопороза и склонность к переломам костей. Часто диагностируются психические расстройства (депрессия или когнитивные нарушения).
Диагностика синдрома Кушинга
Базой диагностики болезни Иценко-Кушинга является сбор анамнеза. При наличии визуальных симптомов возникает подозрение на наличие патологического процесса. Ключевыми в постановке диагноза становятся лабораторные исследования мочи и крови, а также анализ слюны на наличие кортизола.
Кроме того, диагностика болезни Иценко-Кушинга требует направления пациента на компьютерную томографию или МРТ, чтобы определить причину нарушений.
Лечение синдрома Иценко-Кушинга
Лечение синдрома Кушинга зависит от причины заболевания. Если диагностирована опухоль, то требуется операция. Дополнительно необходимо лечить сопутствующие заболевания, например, гипертонию.
Как вылечить синдром Кушинга?
- Применять медикаментозную терапию, которая направлена на блокаду избыточной выработки кортикостероидов и АКТГ.
- Использовать лучевую терапию, снижающую активность гипофиза.
- При длительном приеме кортикостероидов — сократить дозу.
При лечении синдрома Кушинга следует учесть индивидуальность каждого случая, что подразумевает выбор наиболее подходящей терапии.
Операции при синдроме Кушинга
Опухоли гипофиза и надпочечников удаляют хирургическим путем. Если процедура будет проведена радикально, скорее всего исчезнут симптомы болезни. Если пациенту удалили надпочечники, потребуется пожизненная заместительная терапия специальным гормоном. Когда позволяет ситуация, хирург старается применить миниинвазивные методы.
Контроль излеченности
Независимо от вида применявшегося лечения, пациенты с синдромом Иценко-Кушинга нуждаются в длительном динамическом наблюдении. При контрольных обследованиях необходимо оценить:
- эффективность проведенного лечения;
- наличие / отсутствие рецидива заболевания;
- состояние гипофизарных функций.
Наиболее часто после проведенного лечения выпадает функция СТГ, реже — развивается вторичный гипотиреоз, а также появляется нарушение менструальной функции у женщин.
Профилактика
Первичная профилактика синдрома Кушинга не разработана.
Цель вторичной профилактики — предотвратить рецидив болезни. При этом важно соблюдать рекомендации врача, выработать правильный режим дня и пересмотреть рацион питания. Боли в суставах и мышцах лучше снимать с помощью горячей ванны или массажа. Нельзя игнорировать приступы депрессии.
Советы и рекомендации
У людей с синдромом Кушинга часто имеются проблемы в виде диабета или плохой толерантности к глюкозе. Поэтому в основе диеты должны быть макаронные изделия, рис и крупы. Стоит ограничить потребление простых углеводов: сладостей, фруктов, сухофруктов и меда.
Рекомендуемый прием пищи 3-4 раза в день, но не чаще, чем каждые 4 часа. Это позволит избежать постоянной стимуляции поджелудочной железы.
Глюкокортикоиды, которые обычно используют при лечении синдрома Кушинга, увеличивают выведение кальция, цинка и калия. Чтобы восполнить их нехватку, стоит включить в рацион семечки, шпинат, фундук, рыбу и мак.
Статья носит информационно-ознакомительный характер. Пожалуйста, помните: самолечение может вредить вашему здоровью.
Источник
Синдром Кушинга: как поставить диагноз
В каких случаях врач общей практики должен заподозрить синдром Кушинга? Как подтвердить диагноз? Нужно ли отменять короткие курсы экзогенных кортикостероидов постепенно? Рисунок 1. Плетора и лунообразность лица, присущие синдрому К
В каких случаях врач общей практики должен заподозрить синдром Кушинга?
Как подтвердить диагноз?
Нужно ли отменять короткие курсы экзогенных кортикостероидов постепенно?
 |
| Рисунок 1. Плетора и лунообразность лица, присущие синдрому Кушинга |
Есть прекрасное определение, позволяющее различить синдром Кушинга (СК) и болезнь Кушинга (БК). Описанный впервые Гарви Кушингом в 1912 году, синдром Кушинга объединяет симптомы, вызываемые постоянно повышенным уровнем свободного кортизола в крови. Понятие «болезнь Кушинга» оставлено за особым гипофизарным АКТГ-зависимым подтипом синдрома.
Ярко выраженный СК не представляет особых диагностических трудностей, но заболевание с умеренными проявлениями может вызвать у врача общей практики ряд проблем. Диагноз ставится клинически, а подтверждается данными лабораторных исследований.
Большинство случаев СК имеет ятрогенное происхождение и обусловлено длительным приемом преднизолона, дексаметазона или других кортикостероидов. К развитию клинических проявлений заболевания приводит ежедневное применение кортикостероидов в дозах, превышающих эквивалент 7,5 мг преднизолона.
Детям для развития кушингоидных черт достаточно меньших доз.
Хотя СК встречается относительно редко, любой врач общей практики сталкивается с его ятрогенными случаями, вызванными длительным приемом кортикостероидов по поводу таких распространенных заболеваний, как, например, ревматоидный артрит.
Таблица 1. Симптомы синдрома Кушинга (в порядке частоты встречаемости)
БК — наиболее распространенная причина неятрогенного СК (70%); оставшиеся 30% приходятся на случаи эктопической секреции АКТГ и надпочечниковое происхождение болезни (АКТГ-независимый СК).
Клиническая картина. Симптомы СК (см. табл. 1) могут, в зависимости от причины, развиваться остро или исподволь в течение нескольких лет.
Как правило, симптомы неспецифичны и включают сонливость, депрессию, увеличение веса, жажду, полиурию, слабость, легкость появления синяков и гирсутизм [1].
К классическим признакам СК у взрослых относятся «лунообразное» лицо (рис. 1), центральное ожирение (рис. 2), плетора лица, буйволиный горб, надключичные жировые подушечки и периферические отеки. У детей самым ранним признаком служит задержка роста; нормальная кривая роста фактически исключает СК [2].
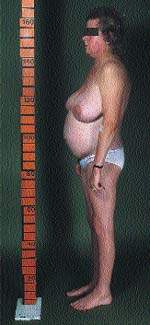 |
| Рисунок 2. Типичная конституция пациента с СК. Обратите внимание на центральное ожирение и относительно тонкие руки и ноги, что вызвано проксимальной миопатией |
Конечно, ожирение в общей практике встречается часто, и трудность состоит в том, чтобы отличить общее ожирение от центрального. Главным признаком является накопление жира в центральной части тела с одновременной его потерей на бедрах, ягодицах и руках. Атрофия поперечнополосатых мышц обусловливает внешний вид пациента, подобный «лимону на палочках».
Еще одним клиническим признаком СК служат истончение кожи и ломкость капилляров, приводящие к легкому и часто спонтанному образованию синяков. Таким больным присущи кожные инфекции, например отрубевидный лишай, молочница и онихомикоз, причем кожные повреждения заживают с трудом. Почти всегда можно обнаружить абдоминальные стрии, развивающиеся вторично за счет центрального ожирения (рис. 3).
Больные могут страдать от гирсутизма вследствие избыточного образования надпочечниковых андрогенов под воздействием повышенного АКТГ.
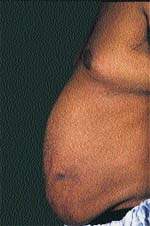 |
| Рисунок 3. Стрии живота у мужчины с СК |
Метаболические изменения, вызываемые повышенным уровнем кортизола, приводят к развитию сахарного диабета, гипертензии и дислипидемии. С длительным повышением циркулирующего в крови кортизола связано также уменьшение минеральной плотности костей и остеопороз.
Биохимическое подтверждение. Важно исключить использование кортикостероидных препаратов и злоупотребление алкоголем («алкогольный псевдо-Кушинг»).
Применение стероидных ингаляторов (например, беклометазона в дозе 200 мкг каждые 6 часов в течение более чем трех месяцев) и других местных стероидных препаратов может приводить к значительному системному всасыванию и развитию клинических проявлений СК с подавлением гипоталамо-гипофизарно-адреналовой оси.
Если пациент не принимает подобных лекарств, первым шагом будет подтверждение избытка кортизола путем определения свободного кортизола мочи (СКМ) в двух суточных пробах [3].
Следующая задача — показать, что эндогенная секреция кортизола не подавлена экзогенными глюкокортикоидами. Для этого проводится ночная дексаметазоновая проба (ДП): в 11 часов вечера пациент принимает 1 мг дексаметазона, а на следующее утро между 8 и 9 часами берется проба крови на кортизол. СК предполагается в том случае, если уровень кортизола не упал ниже 50 нмоль/л. Однако вследствие низкой специфичности теста могут быть ложноположительные результаты.
Направление к специалисту. При подозрении на СК необходимо сразу же направить пациента к эндокринологу. После направления, как правило, дважды проводится определение СКМ и выполняется более специфическое исследование — проба с дексаметазоном в низкой дозе (ДПНД) [4]. Пациент принимает по 0,5 мг дексаметазона восемь раз каждые 6 часов. Отсутствие падения кортизола ниже 50 нмоль/л в 9 часов утра по окончании ДПНД указывает на СК.
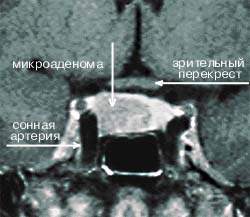 |
| Рисунок 4. МР-томограмма гипофиза, на которой видна правосторонняя микроаденома, секретирующая АКТГ (гипофиз-зависимая болезнь Кушинга) |
Определение СКМ дает нормальные результаты практически постоянно, если у пациента циклический СК (то есть активность заболевания нарастает и падает в течение недель или месяцев), поэтому данное исследование считается низкочувствительным. Более важная проба — ДПНД, и при обнаружении отклонений от нормы пациента следует направить на дальнейшее обследование.
Амбулаторные исследования включают изучение суточного ритма кортизола (рис. 5), дексаметазоновую пробу с высокой дозой [5] (ДПВД, рис. 6) и определение кортикотропин-рилизинг гормона (КРГ). Подтверждение гипофиз-зависимого заболевания основывается на заборе крови из нижнего каменистого синуса для определения в ней уровня АКТГ и последующего введения КРГ [6, 7]. Как правило, требуется визуализация: компьютерное сканирование надпочечников, чтобы дифференцировать надпочечниковое и АКТГ-зависимое состояние; МР-томография гипофиза (рис. 4); компьютерное сканирование грудной клетки и брюшной полости при подозрении на эктопическую секрецию АКТГ.
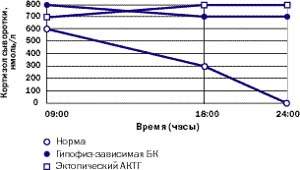 |
| Рисунок 5. Так выглядит типичный суточный ритм кортизола у здорового человека, пациента с БК и пациента с эктопическим СК |
Лечение СК зависит от причины заболевания. Методом выбора при БК служит селективная транссфеноидальная микроаденомэктомия: излечения удается добиться в 80% случаев (эффективным лечение считается тогда, когда наличие кортизола через 24-48 часов после операции не обнаруживается) [8].
При успешном исходе операции по поводу БК пациенту понадобится заместительный курс гидрокортизона, пока не восстановится его собственная гипоталамо-гипофизарно-надпочечниковая (ГГН) функция. Как правило, достаточно 20 мг гидрокортизона утром и 10 мг — в 6 часов вечера.
В случае обнаружения аденомы надпочечников показана односторонняя адреналэктомия. Железа с другой стороны оказывается атрофичной (по принципу обратной связи) в результате длительного подавления секрецией АКТГ, поэтому пациенту также понадобится заместительная терапия гидрокортизоном вплоть до восстановления ГГН.
Эктопические АКТГ-секретирующие опухоли (например, карциноиды бронхов или тимуса) требуют удаления. После операции вновь проводится гидрокортизоновое прикрытие. Процесс включения ГГН может занять несколько месяцев. При отсутствии эффекта от операции проводят облучение гипофиза из внешнего источника (4500 Гр в 25 сериях).
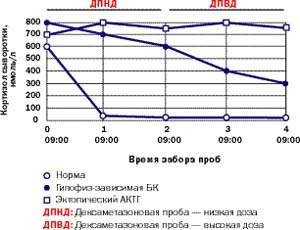 |
| Рисунок 6. Типичные реакции кортизола на дексаметазоновую супрессию низкими (0,5 мг каждые 6 часов в течение 48 часов) и высокими дозами (2 мг каждые 6 часов в течение 48 часов) у здорового человека, пациента с БК и пациента с эктопическим СК |
Если есть противопоказания к проведению оперативного вмешательства, связанные непосредственно с СК, снизить уровень кортизола можно кетоконазолом (начиная с 200 мг). Дозы препаратов подбирают индивидуально, ориентируясь на средний уровень кортизола 200-300 нмоль/л.
После медикаментозного лечения пациент может успешно перенести операцию. При отказе от операции остается возможность длительного лечения кетоконазолом, проводящимся под наблюдением госпитального эндокринолога.
Двусторонняя адреналэктомия проводится только в самых тяжелых случаях, когда безуспешно испробованы все остальные методы. Она неизбежно приводит к необходимости пожизненной заместительной терапии кортикостероидами и минералокортикоидами.
Ведение больных с СК. Самая распространенная причина СК — ятрогенная, особенно если доза принимаемых внутрь стероидов превышает эквивалент 7,5 мг преднизолона у взрослых.
Для профилактики остеопороза пациентам, принимающим стероиды более шести месяцев, назначают бисфосфонаты.
Решение о снижении дозы стероида следует принимать, проконсультировавшись с соответствующим специалистом. Экзогенные стероиды, назначаемые коротким курсом (менее 6 недель), редко вызывают клинически значимую надпочечниковую супрессию, поэтому их можно резко отменять.
При подозрении на неятрогенный СК измерение СКМ и ночная ДП могут помочь в подтверждении этого диагноза (vide supra). Но пациента, у которого обнаружены клинические признаки неятрогенного СК (см. табл.), рекомендуется обязательно направить к эндокринологу.
Случай из практики
Друзья и члены семьи 24-летней женщины заметили, что она полнеет и как бы «сама не своя». Она часто находилась в подавленном настроении и с трудом могла сосредоточиться на своей работе.
Врач общей практики, к которому она обратилась, отметил «лунообразное лицо» и умеренный гирсутизм. Артериальное давление, прежде нормальное, составляло 150/100 мм рт. ст.
Она была срочно направлена к эндокринологу по месту жительства. При обследовании выявлена повышенная суточная экскреция с мочой свободного кортизола и потеря суточного кортизольного ритма. Дексаметазоновая проба не выявила супрессии ни при низкой, ни при высокой дозе дексаметазона; реакция кортизола на экзогенный КРГ оказалась плоской.
МРТ-скан гипофиза был нормальным, а при компьютерном сканировании брюшной полости обнаружены утолщенные гиперплазированные надпочечники, характерные для АКТГ-зависимости. Пигментация ладонных складок также подтверждала повышение продукции АКТГ.
Был поставлен клинический и биохимический диагноз эктопического АКТГ-синдрома, и больную отправили в соответствующий центр. Компьютерное сканирование грудной клетки выявило опухоль размером 1 см в верхушке правого легкого, которая была удалена под прикрытием гидрокортизона.
После четырехмесячного курса преднизолона (5 мг на ночь и 2,5 мг днем) наблюдалось восстановление ее ГГН-оси, и стероиды постепенно отменили. Тело приобрело нормальные формы в течение 6 месяцев, восстановилась супрессорная активность дексаметазона.
Источник
