- Методологические аспекты доклинической оценки противоопухолевой активности на примере оригинального цитостатика у крыс Wistar с трансплантируемой карциносаркомой Walker 256
- Резюме
- Материал и методы
- Заключение
- Благодарности
- Вклад авторов
- Крысы линейные Wistar
- Прайс-лист на поставку линейных крыс Wistar
- Детальный Прайс-лист на нашу продукцию
- Характеристики крыс линии Wistar
- Примеры экспериментов, проводимых на линейных крысах Wistar
- Где приобрести
Методологические аспекты доклинической оценки противоопухолевой активности на примере оригинального цитостатика у крыс Wistar с трансплантируемой карциносаркомой Walker 256
Я.Г. Муразов, канд. биол. наук., научный сотрудник научной лаборатории химиопрофилактики рака и онкофармакологии, ORCID: 0000-0002-6573-3112;
А.Н. Стуков, доктор мед. наук, старший научный сотрудник научного отдела инновационных методов терапевтической онкологии и реабилитации, ORCID: 0000-0002-1741-6630;
Ю.Г. Змитриченко, младший научный сотрудник научной лаборатории химиопрофилактики рака и онкофармакологии, ORCID: 0000-0002-9137-9532;
Г.В. Точильников, канд. мед. наук, и.о. заведующего научной лаборатории химиопрофилактики рака и онкофармакологии, ORCID: 0000-0003-4232-8170
ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
197758, Россия, г. Санкт-Петербург, пос. Песочный, ул. Ленинградская, д. 68
Резюме
В статье представлены основные количественные показатели, используемые для доклинической оценки фармакологической активности перспективных средств противоопухолевой терапии. В качестве примера приведены результаты изучения терапевтической активности отечественного цитостатического соединения хлонизол на модели трансплантируемого штамма-аллографта (карциносаркома Walker 256) у крыс линии Wistar. После подкожной трансплантации в бедро 0,5 мл 10% взвеси опухолевых клеток в 0,9% растворе натрия хлорида, 25 половозрелых крыс-самцов Wistar были рандомизированы на 2 группы: крысам 1-й (контроль; n=15) внутрибрюшинно вводили 0,5 мл 0,9% раствора натрия хлорида; животным 2-й группы (хлонизол; n=10) внутрибрюшинно вводили тестируемое соединение в дозе 15 мг/кг (75% максимально переносимой дозы) в 0,9% растворе натрия хлорида. Введение осуществляли на 6-й день после трансплантации, когда опухоль определялась визуально и пальпаторно у всех животных. Во время эксперимента определяли следующие параметры: торможение роста опухоли (Т%), кинетику роста опухоли, общую выживаемость (ОВ) и индекс роста опухоли (ИРО). Под влиянием хлонизола наблюдалась значительная регрессия опухолей (непарный t-критерий; P мг/кг статистически значимо увеличивало медиану ОВ в сравнении с контролем с 15 дней до 60,5 дней (логранговый критерий; P в конечном итоге скажется на экономических затратах разработчика в целом.
По разным причинам для изучения противоопухолевой активности в экспериментах in vivo наибольшее распространение получили модели опухолей у грызунов. Использование этих животных для оценки противоопухолевой активности подвергается критике из-за наличия случаев, когда соединение продемонстрировало эффективность у грызунов, но впоследствии было неэффективным у человека. Тем не менее существует >100 одобренных для клинического применения соединений, которые продемонстрировали эффективность на моделях опухолей у грызунов [5]. В рутинной доклинической практике для оценки эффективности химиотерапевтических агентов наиболее часто используются перевиваемые мышам и крысам опухолевые штаммы различного гистогенеза (сингенные и линейно-неспецифические) и ксенографты человека (PDX-модели (patient-derived xenograft) и клеточные линии). Для решения специальных задач могут быть использованы модели индуцированного канцерогенеза (химический, радиационный) или трансгенные животные [6]. Сингенные и линейно-неспецифические штаммы опухолей грызунов используются для оценки спектра противоопухолевой активности с определением оптимальной схемы лечения и отработки оптимальных фармакологических параметров (доз, режимов). Ксенографты человека используются для доказательства эффективности тестируемого соединения при тех или иных опухолях у человека, трансплантируемых иммунодефицитным мышам. Изучение влияния исследуемого агента на метастатический потенциал проводится с использованием моделей метастазирующих опухолей.
В статье представлены результаты изучения перспективного цитостатического агента (хлонизола), синтезированного в ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, на модели трансплантируемой карциносаркомы Walker-256 у крыс Wistar. Описаны методологические аспекты оценки противоопухолевой активности.
Материал и методы
Характеристика тестируемого объекта. Хлонизол (2-[3-(2-хлорэтил)-3-нитрозоуреидо]-1,3-пропандиол) относится к классу нитрозоалкилмочевин (НАМ) (рис. 1). Молекулярные механизмы действия НАМ связаны с алкилированием и карбомоилированием макромолекул продуктами биодеградации соединений. По уровню цитогенетической активности хлонизол превосходит все другие исследованные ранее препараты класса НАМ [7, 8].
Карциносаркома Walker-256 – один из наиболее часто используемых трансплантируемых штаммов в доклинических исследованиях. Впервые описана G. Walker в 1928 г. Карциносаркома Walker-256 возникла в результате спонтанного канцерогенеза в молочной железе у беременной крысы-альбиноса. Опухоль полностью регрессировала в период лактации, но выросла снова после отлучения потомства от груди [9]. После перевивки опухоль демонстрирует агрессивное биологическое поведение – способна к локальной инвазии и метастазированию, в т.ч. в кости [10]. С целью индукции солидной опухоли трансплантация штамма выполнялась под кожу боковой поверхности бедра в виде 10% опухолевой взвеси в 0,9% растворе натрия хлорида. Объем введения взвеси – 0,5 мл.
Животные. Эксперимент был проведен на 25 половозрелых аутбредных крысах-самцах Wistar, полученных из ФГУП «Питомник лабораторных животных «Рапполово» (Ленинградская обл., Россия) с медианой начальной массы тела 320 г (min/max 305–381 г). Размер выборки был рассчитан на основании анализа выживаемости животных в предыдущем разведочном исследовании. Было достаточно по 10 животных в группе, чтобы отклонить нулевую гипотезу, о том, что выживаемость в контрольной группе и группе хлонизола одинакова с мощностью (1-β)=80% и α=0,05 [11]. Увеличение в группе контроля числа животных до 15 обусловлено дизайном всей программы фармакологических исследований хлонизола. Уход и все манипуляции с животными выполнялись в соответствии с Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях (ETS N 123), Директивой Европейского парламента и Совета Европейского Союза 2010/63/ЕС о защите животных, используемых для научных целей. Протокол был одобрен локальным этическим комитетом. Животные содержались в конвенциональном виварии в стандартных условиях: температура воздуха 20–24°C, относительная влажность 50–60%, 12-часовой цикл светлого/темного времени суток. Крысы получали полнорационный брикетированный комбикорм производства компании «Лабораторкорм» (Москва, Россия) и водопроводную питьевую воду ad libitum.
Дизайн эксперимента. На 6-й день после трансплантации опухоли животные были рандомизированы на две группы: крысам 1-й (контроль; n=15) внутрибрюшинно вводили 0,5 мл 0,9% раствора натрия хлорида; животным 2-й группы (хлонизол; n=10) внутрибрюшинно вводили тестируемое соединение в дозе 15 мг/кг (75% максимально переносимой дозы) в 0,9% растворе натрия хлорида. Введение препаратов на 6-й день после трансплантации опухоли было необходимо для оценки эффектов хлонизола на сформировавшуюся опухоль.
Оцениваемые параметры. Наблюдение за животными-реципиентами осуществляли в течение всего периода жизни. При оценке противоопухолевого эффекта хлонизола использовались следующие критерии:
1. Объем опухоли и кинетика роста. Объем опухоли в каждой временнóй точке определяли по формуле:
где А – наибольший диаметр опухоли, В – перпендикулярный ему диаметр.
2. Торможение роста опухоли (Т%) оценивали по формуле:
где VK – средний объем опухоли у крыс контрольной группы, VЭ – средний объем опухоли у крыс экспериментальной группы, получавших хлонизол; Т% – процент торможения роста опухоли.
3. Индекс роста опухоли (ИРО). Является интегральными показателем противоопухолевой активности с учетом не только выраженности противоопухолевого эффекта, но и его устойчивости [12]. ИРО определяли в процентах по формуле:
где Sэ – площадь под кинетической кривой роста опухоли в группе крыс, получавших терапию,
a SК – площадь под кинетической кривой роста опухоли крыс контрольной группы.
Для измерения площади под кинетической кривой роста опухоли использовали метод трапеций, базирующийся на формуле:
где Vi – объем опухоли в соответствующем измерении под номером i; n – число измерений; время в днях: t1 – между первым и вторым измерениями, t2 – между вторым и третьим измерениями, tn-1 – между предпоследним и последним измерениями.
4. Общую выживаемость (ОВ) определяли как время со дня перевивки опухоли до дня гибели животного. Критерием полного излечения считали продолжительность жизни >90 дней.
Статистический анализ. Статистическую обработку результатов эксперимента проводили с помощью пакета GraphPad Prism версии 8.0 и jamovi версии 1.6.12. Количественные данные представлены в виде среднего (±стандартная ошибка среднего, SEM). Критерий Левина использовали для оценки равенства дисперсий. Непарный t-критерий Стьюдента использовали для сравнения количественных данных. Для сравнения категориальных переменных применяли точный критерий Фишера. Данные по ОВ животных графически представлены в виде кривых Каплана–Мейера. Для сравнения кривых ОВ применяли логранговый критерий. Все критерии были двусторонними. Различия считались статистически значимыми при р 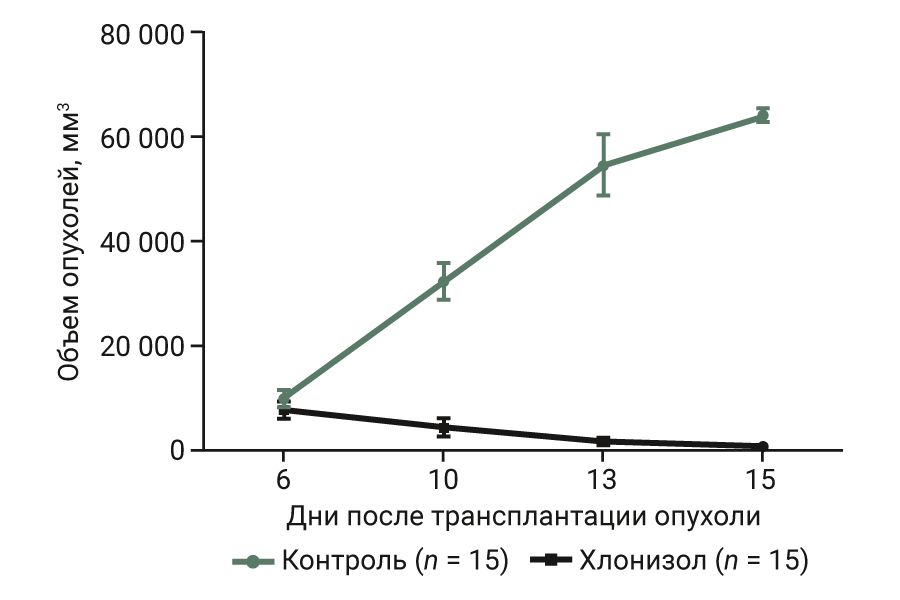
В данной серии экспериментов изучали активность хлонизола в дозе 15 мг/кг, что составляет 75% от максимально переносимой дозы (МПД). МПД у крыс при однократном введении составила 20 мг/кг [13]. Для оценки влияния хлонизола на развившуюся опухоль лечение начинали на 6 день после трансплантации карциносаркомы Walker-256.
Профиль кинетической кривой демонстрировал выраженную противоопухолевую активность хлонизола в сравнении с контролем (рис. 2).
Под влиянием хлонизола наблюдалась значительная регрессия опухолей (табл. 1), которая у 5 из 10 животных оказалась полной и сохранялась в течение 90 дней наблюдения.
Результаты определения площади под кинетической кривой роста опухоли и ИРО представлены в табл. 2. Установлено, что в группе хлонизола эти показатели значимо были ниже в сравнении с контрольной группой.
Кривые общей выживаемости крыс в эксперименте представлены на рис. 3. Введение хлонизола в дозе 15 мг/кг статистически значимо увеличивало медиану ОВ в сравнении с контролем с 15 дней до 60,5 дней (логранговый критерий; P 24-му дню после перевивки все крысы контрольной группы (n=15) погибли от прогрессирования опухоли, все крысы, получившие хлонизол (n=10), к этому сроку оставались живы. У 5 из 10 животных, получивших хлонизол, опухоли полностью регрессировали. Эти крысы пережили 90 дней без признаков рецидивов, что может рассматриваться как полное излечение. Разница с контролем статистически значима (точный критерий Фишера; р=0,0047).
Заключение
В представленной работе описаны основные количественные показатели, используемые для оценки эффективности химиотерапевтических агентов на примере оригинальной молекулы и одного перевиваемого штамма-аллографта у крыс. Эти показатели могут быть использованы и для оценки эффективности других перспективных противоопухолевых агентов (таргетных препаратов, средств иммунотерапии). Карциносаркома Walker-256 у крыс обладала высокой чувствительностью к хлонизолу. При позднем начале лечения (на 6 день после трансплантации), когда у всех животных уже имелись сформировавшиеся опухоли, введение хлонизола привело к излечению 50% животных. Результаты проведенного эксперимента дополняют ранее полученные сведения о высокой противоопухолевой активности хлонизола на моделях трансплантируемых опухолей.
Благодарности
Работа выполнена без спонсорской поддержки.
Вклад авторов
Муразов Я.Г. – концепция, сбор и систематизация материала, написание, редактирование текста статьи.
Стуков А.Н. – сбор и систематизация материала, критические замечания.
Змитриченко Ю.Г. – сбор и систематизация материала.
Точильников Г.В. – редактирование текста статьи.
Источник
Крысы линейные Wistar
Эксперименты с использованием лабораторных животных – один из наиточнейших методов испытаний в различных сферах: биологической, фармакологической, ветеринарной, косметической, военной, космической и многих других. Для подобных исследований подходят многие животные, по крайней мере, о специально выведенных особях не слышали ни в XIX, ни в XX веках, но в настоящее время испытания проводятся на ответвлениях видов грызунов и др. зверей, подготовленных для лабораторий. К ним относятся и крысы линейные Wistar.
Прайс-лист на поставку линейных крыс Wistar
| Вес | Цена, руб. |
|---|---|
| до 40 гр. | 380 |
| 40 — 60 гр. | 399 |
| 60 — 80 гр. | 428 |
| 80 — 100 гр. | 456 |
| 100 — 120 гр. | 494 |
| 120 — 140 гр. | 546 |
| 140 — 160 гр. | 570 |
| 160 — 180 гр. | 589 |
| 180 — 200 гр. | 618 |
| от 200 гр. | 656 |
Детальный Прайс-лист на нашу продукцию с указанием цен на все виды лабораторных животных мы вышлем вам по электронной почте. Для заказа оставьте свои контактные данные и нажмите кнопку «Получить Прайс-лист» в секции ниже.
Детальный Прайс-лист на нашу продукцию
Характеристики крыс линии Wistar
- окрас – альбиносы, полностью белые;
- масса тела – 150-400 граммов у взрослой особи;
- половое созревание в течение 2 месяцев;
- беременность – 3 недели;
- количество новорожденных от 6 до 12;
- широкая объёмная голова и длинные уши;
- короткий, относительно тела, хвост.
Это знаменитая инбредная линия, созданная в институте в Филадельфии, от которой пошли остальные линии подопытных крыс, используемых в настоящее время. Сейчас существует около 1000 линий, и к ним относятся: аутбредные и инбредные, а также трансгенные и нокаутные.
Из-за простоты и низких затрат на содержание, и скорого размножения линейные крысы очень востребованы в качестве модельных организмов. Сегодня животные линии Wistar заняты в исследованиях продуктов питания, токсикологических, на них проверяют действие гормональных препаратов. Задействованы они также и при изучении инфекционных заболеваний, доброкачественных и злокачественных опухолей.
Примеры экспериментов, проводимых на линейных крысах Wistar
Вследствие схожести многих процессов у крыс и человека, на первых проводится изучение поведения людей в определённых обстоятельствах. Одним из экспериментов, проводимых в лабораторных условиях, стало исследование поведения животных в нормальном состоянии и при остром абстинентном синдроме, сиречь похмелье. Изучение этой проблемы с участием линейных крыс Wistar в будущем позволит не только купировать неадекватное поведение, но и, вообще, снять вопрос самого синдрома. Результаты эксперимента следующие:
- Двигательная активность животных с абстинентным синдромом отличалась от активности контрольной группы, чувствовалась неуверенность движений.
- Экспериментальные крысы были более напряжены эмоционально, чем контрольные, нередко срываясь на соратниках.
- Мозг абстинентников работал менее чётко, чем у проверочной группы животных, что приводило к ошибкам в прохождении секторов для получения пищи.
- При применении некоторых лекарственных препаратов, уровень реагирования крыс с абстинентным синдромом повышался, напряжённость спадала.
Благодаря наблюдениям за крысами линии Wistar, появились новые возможности для реабилитации подверженных действию этанола людей.
Где приобрести
Партию крыс линейных Wistar купить можно в биопитомнике «СТЕЗАР», как и других подопытных животных. Продукты компании сертифицированы и соответствуют международным нормам. Крысы и другие грызуны, которых поставляет питомник, выращены в чистой природной зоне, клинически здоровы и не являются носителями вирусов, болезнетворных бактерий и паразитов.
Каждая партия животных соответствует запрошенной породе, полу и весу, и по количеству не отличается от заказа. Гарантия во всех случае распространяется на крыс, мышей, морских свинок и др. в течение всего срока действия договора. Доставка же производится согласно правилам перевозки скоропортящихся грузов.
Источник


