- Папилломатоз шейки матки
- Что такое папиллома?
- Чем опасен вирус папилломы человека
- Чем опасен вирус папилломы человека
- Когда возникает онкология?
- Причины развития папиллом шейки матки
- Симптомы папилломатоза
- Диагностика папилломатоза
- Лечение папилломатоза
- Возможно ли удаление папиллом влагалища и шейки матки лазером?
- Папилломы на интимных местах
- Причины появления папиллом
- Пути заражения
- Вероятность заражения
- Симптомы
- Диагностика
- Лечение
- Современные подходы к лечению папилломавирусной инфекции урогенитального тракта
- Структура вирусного генома
- Клиника ПВЧ-инфекции
- Принципы лечения ПВЧ-инфекции
- Деструктивные методы
- Физические деструктивные методы
- Специфическая противовирусная терапия
- Цитотоксические препараты
- Иммунологические методы
- Таблица 1. Аногенитальная ВПЧ-инфекция и ассоциированные с ВПЧ заболевания
- ВПЧ-инфекция
Папилломатоз шейки матки
На сегодняшний день ВПЧ является наиболее распространенным из всех заболеваний, передающихся половым путем. Вирусом папилломы человека заражены около 50% всего населения земли. В настоящее время насчитывается около 180 типов ВПЧ, из них 29 типов обладают онкогенным потенциалом. По степени онкогенного риска выделяют следующие группы ВПЧ:
- ВПЧ «низкой степени» риска;
- ВПЧ «средней степени» риска;
- ВПЧ «высокой степени» риска.
Инкубационный период заболевания составляет от 1-го до 12-ти месяцев.
Что такое папиллома?
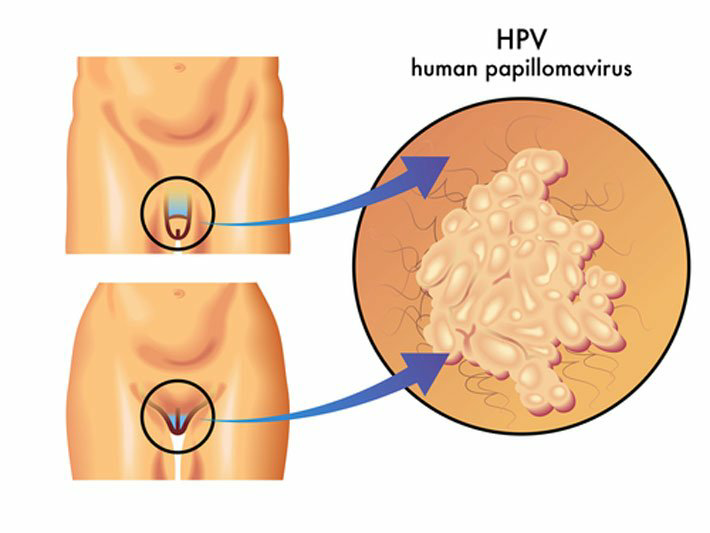
Папиллома выглядит как небольшой нарост (бородавка) телесного, розоватого или коричневатого цвета, на тонкой ножке. Она может достигать в размере 1-2 см. При обильном разрастании папилломы внешне напоминают структуру цветной капусты и, чаще всего, располагаются на половых органах, но могут появиться и в любом другом месте. У женщин они располагаются в области больших и малых половых губ, реже возникают папилломы шейки матки и влагалища.
Остроконечные кондиломы, вагинальные папилломы локализуются, в основном, в местах трения и травматизации при половом контакте. У женщин поражаются уздечка половых губ, большие и малые половые губы, клитор, уретра, лобок, промежность, перианальная область, преддверие и вход во влагалище, а также девственная плева, непосредственно влагалище и шейка матки. В уретре кондиломы располагаются кольцеобразно, главным образом в области наружного отверстия.
Чем опасен вирус папилломы человека
Знакомые многим папилломы, или бородавки, возникают в результате активности вируса, которым инфицирована значительная часть мирового населения. Вирус папилломы человека (ВПЧ) становится причиной появления специфических выростов не только на поверхности кожи, но также на слизистых оболочках (например, папиллома шейки матки) и в так называемых «пограничных» областях между слизистыми и эпителием кожи (например, кондиломы в области ануса и входа во влагалище).
Чем опасен вирус папилломы человека
Выросты на коже и слизистых оболочках, в зависимости от размера и расположения, часто бывают причиной ощутимого дискомфорта:
- неэстетичный вид образований;
- раздражение, воспаление и зуд в пораженной области;
- кровотечение из поврежденных папиллом.
Но они представляют собой не только эстетическую проблему, но и потенциальную угрозу жизни и здоровью. Папиллома шейки матки основная причина рака шейки матки.
Когда возникает онкология?
Количество разных типов вируса папилломы человека достигает 180, и только 29 из них имеют доказанную способность провоцировать появление злокачественно изменённых клеток. Такие типы вируса называют «онкогенными». Наличие папилломы шейки матки, бородавок в области ануса и гениталий в любом случае должно стать поводом для начала лечения у хорошего специалиста, обязательных диагностических и лечебных процедур (лабораторное выявление типа вируса, удаление папиллом, коррекция иммунитета и др.).
Причины развития папиллом шейки матки
Заражение вирусом, которое впоследствии приводит к развитию папилломы шейки матки, как правило, происходит половым путем. Инфицирование может происходить также в бассейнах, банях, спортзалах и других общественных местах и в результате самозаражения при бритье, эпиляции, обкусывании ногтей, расчесах кожи.
Наблюдается также перенос вируса при папилломе шейки матке от родителей к детям. Новорожденные могут быть инфицированы в родах при прохождении через родовые пути матери, которая не прошла лечение папиллом влагалища, половых губ или шейки матки.
К группе риска заражения папилломой шейки матки относятся все женщины, живущие половой жизнью. Факторами риска развития инфекции являются:
- раннее начало половой жизни;
- большое количество половых партнеров;
- местные раздражители (выделения из влагалища, уретры, прямой кишки при различных патологических состояниях, мацерация, скопление смегмы и т. д);
- дисбиотические состояния;
- курение, алкоголь;
- авитаминоз и атопический дерматит;
- беременность;
- лечение цитостатиками;
- контакт с женщиной, больной раком шейки матки или имеющей папилломы в матке;
- лечение папиллом в шейке матка (2 раза)
- сочетание требующей лечения папилломы шейки матки с другими ИППП (хламидиоз, урогенитальный микоплазмоз, гонорея, трихомониаз, бактериальный вагиноз, HSV-инфекция, ВИЧ, цитомегаловирусная инфекция, сифилис и т.д.).
Симптомы папилломатоза
Сложность диагностики и лечения папиллом шейки матки заключается в том, что данное заболевание может протекать практически бессимптомно! Тем не менее, некоторые пациенты отмечают косвенные признаки ВПЧ, к которым относятся:
- болезненность при половом акте;
- кровянистые выделения после полового акта;
- резкий, неприятный запах из половых органов.
Диагностика папилломатоза
Диагноз «папилломатоз шейки матки» ставится на основании клинического осмотра, расширенной кольпоскопии, цитологического и гистологического исследования. Обязательным является обследование пациентов на наличие сопутствующих ИППП.
Обнаруженные при осмотре шейки матки в зеркалах и при расширенной кольпоскопии эктопия и лейкоплакия, являются обязательным показанием для обследования на ВПЧ. Наибольшее диагностическое значение в настоящее время придается методу полимеразной цепной реакции (ПЦР), позволяющий идентифицировать отдельные типы ВПЧ. Этот метод имеет большую прогностическую значимость, особенно если на фоне папилломавирусной инфекции уже имеется картина дисплазии эпителия шейки матки. Новым способом диагностики ВПЧ-инфекции является определение онкобелка Е7 в цервикальном материале методом иммунофлюоресцентного анализа.
Лечение папилломатоза
Лечение заболеваний, вызванных ВПЧ, включает в себя не только уничтожение образований, но и коррекцию общего и местного иммунодефицита, а также устранение факторов, способствующих развитию болезни. Адекватное лечение сопутствующих ИППП следует проводить перед деструкцией кондилом и обязательно на фоне приема иммунокорригирующих препаратов.
В клинике Гинеко для удаления папиллом применяется высокоэффективный и безболезненный метод высокочастотной радиоволновой деструкции.
Возможно ли удаление папиллом влагалища и шейки матки лазером?
В мировой медицинской практике папилломы в гинекологии удаляются хирургическим путем, химическим прижиганием, лазером, однако лучшим и наиболее эффективным методом считается малоинвазивная техника удаления папиллом радиоволновым аппаратом Сургитрон: цена на такую услугу невысока, а сама процедура практически безболезненна и не требует долгого восстановительного периода.
Разумеется, чтобы избежать рецидива, за подобной услугой стоит обращаться только в проверенные клиники, опытный специалист в обязательном порядке проводит диагностику, собирает анализы, чтобы точно установить причины папилломы шейки матки и назначить адекватную схему лечения.
Применение такого оперативного вмешательства в сочетании с индивидуально подобранной иммуномодулирующей и противовирусной терапией позволяет добиться полного выздоровления в короткие сроки.
Мы индивидуально подходим к решению проблем каждой пациентки, учитывая при выборе метода лечения ее возраст, иммунный статус, характер и локализацию заболевания, сопутствующие урогенитальные инфекции. Именно такой подход гарантирует нашим пациенткам высокую эффективность лечения и низкий риск возникновения рецидивов болезни.
В настоящее время, самым многообещающим и перспективным направлением борьбы с ВПЧ является, бесспорно, применение профилактической вакцинации против ВПЧ тех типов, которые являются самыми частыми виновниками рака шейки матки, рака вульвы, рака влагалища.
Источник
Папилломы на интимных местах
Папилломы представляют собой разрастания на коже и слизистых оболочках. Наиболее часто папилломы на интимных местах расположены на коже наружных половых органах и слизистых уретры, влагалища, шейки матки, в области вокруг анального отверстия.
Причины появления папиллом
Причиной появления папиллом на интимных местах является вирус папилломы человека (ВПЧ), циркулирующий в крови почти каждого мужчины и женщины, начиная с подросткового возраста. По данным ВОЗ ВПЧ инфицировано 80-90% населения.
Наиболее часто папилломы встречаются у лиц молодого возраста, имеющих большое количество половых партнеров. Генитально-анальные папилломы – типичные проявления папилломавирусной инфекции. В 90% случаев вызываются шестым и одиннадцатым типами ВПЧ.
В повседневной жизни каждого человека увеличивают риск инфицирования следующие воздействия:
- курение;
- стресс;
- использование чужих гигиенических принадлежностей;
- посещение бань, саун;
- рукопожатие с носителями на этапе обострения;
- снижение иммунитета.
Глобально на распространение ВПЧ влияет множество факторов, в числе которых социально-экономические, медицинские, гигиенические и географические. Вирус может годами находиться в организме, никак себя не проявляя. Провоцирует его активизацию ослабление защитных сил иммунной системы, что и влечет за собой появление папиллом на интимных местах, как у женщин, так и у мужчин.
Беременность, гормональные сбои, нарушение обмена веществ, острые вирусные инфекции, длительные хронические заболевания, плохое питание и недосып могут также спровоцировать рост папиллом на интимных местах.
Пути заражения
Инфицирование возможно не только через половую близость, хотя она является наиболее частой причиной. Заражение ВПЧ также возможно бытовым путем:
- при использовании общих гигиенических и столовых принадлежностей;
- через контакт с инфицированным в стадии обострения при наличии микротравм;
- возможность передачи ВПЧ через бытовые предметы все еще обсуждается.
Редко встречается трансплацентарный путь инфицирования – от матери к ребенку, еще на этапе внутриутробного развития плода.
Вероятность заражения
Примерно в равной степени женщины и мужчины имеют риск стать инфицированными, совершенно не подозревая об этом, поскольку пик заражения приходится на подростковый период и старше, когда снижается настороженность в отношении заражения герпесвирусной, папилломовирусной, ВИЧ-инфекцией.
При этом большее внимание уделяется заболеваниям, передающимся половым путем, которые, тем не менее, также отличаются высокой динамикой заражения.
Важным моментом остается количество половых партнеров, так как на сегодняшний день уже описано более 190 типов ВПЧ и с каждым годом штаммов вируса становится больше. Международное агентство по изучению рака выделяет 12 штаммов, которые связаны с развитием рака различной локализации:
- шейки матки;
- вульвы;
- влагалища;
- анального канала;
- пениса.
Выбирая наименьшее число сексуальных партнеров, риск заразиться ВПЧ, в том числе его онкогенными штаммами, значительно снижается.
Необходимо помнить об индивидуальной гигиене, а также о существовании вакцинации, которая на 95% снижает риск развития ВПЧ. Эффективнее проводить вакцинацию в возрасте до 14 лет, но возможен вариант и до 25 лет. Наибольшую защищенность вакцина дает в случае, если она была введена до начала половой жизни.
Симптомы
При наличии папиллом на интимных местах симптомы делят на субъективные (ощущения, жалобы) и объективные (что непосредственно может увидеть специалист). К субъективным относятся:
- наличие разрастаний (одиночных или множественных);
- пятна на коже и слизистых оболочках половых органов;
- зуд и другие неприятные поверхностные ощущения в области поражения;
- болезненность во время полового акта;
- если мужские папилломы на интимных местах расположены в области уретры, могут наблюдаться жжение и болезненный зуд, нарушение мочеиспускания.
Для патологии характерно наличие болезненных трещин и кровоточивости кожи и слизистых.
К объективным симптомам относятся:
- высыпания;
- папулы и пятна;
- бородавчатоподобные папилломы;
- остроконечные кандиломы, локализованные в промежности и перианальной зоне.
Диагностика
Для того чтобы более достоверно определить, относится ли новообразование к аногенитальным бородавкам, проводится проба с 5% раствором уксусной кислоты, после обработки которым папилломы на интимных местах сохраняют серовато-белую окраску при изменяющемся, усиливающимся сосудистом рисунке нормальной кожи. Также в диагностике могут быть использованы лабораторные исследования – идентификация генотипа ВПЧ с прогнозом течения заболевания.
Для диагностики предраковых состояний на фоне папиллом в интимных местах у женщин рекомендована консультация акушера-гинеколога и уролога при локализации папиллом на интимных местах у мужчин, например, при внутриуретральной локализации. При наличии папилломатозных процессов в анальной области рекомендована консультация проктолога.
Лечение
На вопрос, чем лечить папилломы на интимных местах, современная медицина дает однозначный ответ: их необходимо удалять. Деструкция доброкачественных новообразований может проводиться различными методами:
- электрокоагуляция – воздействие током высокой частоты;
- криодеструкция – удаление с помощью обработки холодом;
- лазерное удаление – послойная обработка излучением лазера;
- химическая деструкция – с помощью специальных химических растворов.
Также возможен вариант классического хирургического удаления.
Конкретную схему, как полноценно и безопасно убрать папилломы на интимных местах, назначает специалист в соответствии с локализацией процесса, тяжестью течения, сопутствующими заболеваниями.
Немаловажный аспект лечения папиллом на интимных местах – это изменение образа жизни и укрепление иммунной системы. Комплексный подход позволяет избежать появления новых образований.
Источник
Современные подходы к лечению папилломавирусной инфекции урогенитального тракта
В последние годы в России, как и во многих странах мира, увеличивается заболеваемость папилломавирусной инфекцией. Проблема ее диагностики и лечения привлекает внимание врачей различных специальностей: дерматологов, гинекологов, урологов, онкологов, пато
В последние годы в России, как и во многих странах мира, увеличивается заболеваемость папилломавирусной инфекцией. Проблема ее диагностики и лечения привлекает внимание врачей различных специальностей: дерматологов, гинекологов, урологов, онкологов, патоморфологов, иммунологов, вирусологов. Это объясняется высокой контагиозностью и тенденцией к росту частоты данного заболевания, а также способностью некоторых разновидностей вируса папилломы человека (ВПЧ) инициировать злокачественные процессы. Последнее большей частью касается генитальных проявлений папилломавирусной инфекции.
Папилломавирус человека (ПВЧ) является эпителиотропным и обнаруживается в кожном покрове, слизистой оболочке рта, конъюнктиве, пищеводе, бронхах, прямой кишке.
В литературе имеются сведения о том, что внедрение ПВЧ-инфекции происходит на уровне незрелых клеток эпителия кожи и слизистых оболочек (базальный слой). Результатом этого внедрения является пролиферация клеток, но без продукции вирусных частиц, поскольку пролиферирующие клетки эпителия не способны поддерживать жизненный цикл вирусов. Полная репликация ПВЧ происходит только в высокоспециализированных клетках многослойного плоского эпителия: зернистых, шиповатых клетах кожи, поверхностных эпителиоцитах слизистой шейки матки. В настоящее время описано порядка 100 типов папилломавирусов. Следует отметить их ткане- и видоспецифичность. Различные типы ПВЧ связаны с различными видами поражений. Установлено, что с урогенитальной областью ассоциированы определенные типы ПВЧ. Выделяются разновидности:
- низкого онкологического риска;
- среднего онкологического риска;
- высокого онкологического риска.
Структура вирусного генома
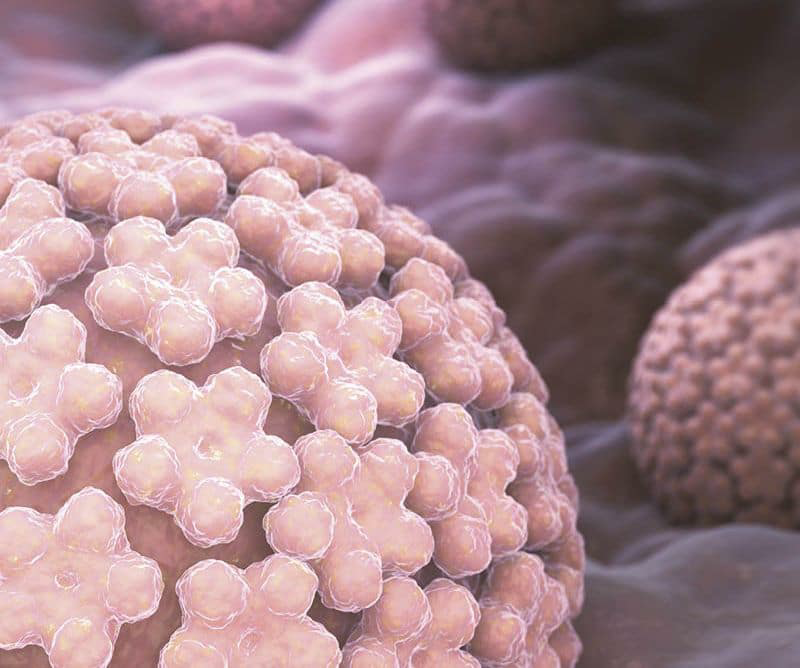
Вирусы папиллом относятся к семейству паповавирусов (Papovaviridae), поражающих крупный рогатый скот, птиц, а также человека и способных инфицировать базальные клетки кожи и плоского эпителия. Папилломавирусы — эта одна из наиболее гетерогенных групп вирусов, критерием дифференциации которой является степень генетического родства вирусов по данным молекулярной гибридизации: она колеблется от 10 до 85%. Диаметр вирусных частиц составляет 55 нм. Вирус не имеет внешней оболочки. Капсид вируса состоит из 72 капсомеров. Детальный анализ молекулы ДНК ВПЧ стал возможен после разработки методики расщепления ДНК с использованием эндонуклеаз и анализа этих фрагментов с помощью гель-электрофореза.
При изучении препаратов, окрашенных по Папаниколау, определен специфический комплекс признаков, характеризующих ядро и цитоплазму эпителиальных клеток (койлоцитарная атипия клеток), обусловленных цитопатическим действием вирусов папиллом.
Специфической клеткой для этой инфекции является койлоцит, представляющий собой оксифилтноокрашенную клетку эпителия с четкими границами и ясно выраженной перинуклеарной зоной просветления и многочисленными вакуолями в цитоплазме.
Термин «койлоцитарная дисплазия» введен H. S. Stegner в 1981 г. Предполагается, что эти изменения являются следствием репродукции вируса, вызывающего нарушение метаболизма клеток, приводящие к их частичному некрозу с образованием баллоноподобных клеток.
Цитологическое исследование очагов, вызванных ПВЧ-инфекцией, показало, что в клеточном материале находятся большей частью безъядерные, или ортокератотические, клетки. Около 20% чешуек содержат ядра — т. наз. «паракератотические клетки».
Следует помнить, что для выявления ПВЧ одной морфологии недостаточно. В этой связи целесообразно использовать метод полимеразной цепной реакции (ПЦР), гибридизацию in situ. В литературе все чаще появляются сообщения об определении ПВЧ-инфекции в моче с помощью ПЦР как альтернативном методе тестирования образцов из шейки матки. Наряду с этим используется гнездовая ПЦР в одной пробирке и типоспецифическая гибридизация нуклеотидов.
Метод ПЦР используется при малосимптомных или асимптомных формах заболевания, вызванного ПВЧ-инфекцией.
Иммунохимическими методами удается выявить антигены ПВЧ в тканях остроконечных кондилом в 71,4% случаев, методом гибридизации — в 96,5% и с помощью ПЦР — в 10% случаев.
Эффективность ДНК-гибридизации не превышает эффективности гистологического исследования, но позволяет выявить пациентов с высокой степенью этой инфекции.
Клиника ПВЧ-инфекции
Клинические проявления ПВЧ-инфекции гениталий очень вариабельны. В настоящее время они подразделяются на остроконечные кондиломы, папиллярные разновидности кондилом (с выраженным экзофитным ростом), а также плоские и инвертированные (внутриэпителиальные) с эндофитным ростом. Последний вариант, известный также под названием «субклиническая ПВЧ-инфекция», наиболее сложен в диагностическом плане, поскольку отсутствуют четкие микроскопические изменения эпителия. В этом случае для определения четких границ поражения требуются специальные скрининговые приемы.
Своеобразным вариантом остроконечных кондилом является бовеноидный папуллез и гигантская кондилома Бушке — Левенштейна. Остроконечные кондиломы (ОК) представляют собой фиброэпителиальное образование на поверхности кожи и слизистых, с тонкой ножкой или широким основанием в виде единичного узелка или множественных эпителиальных выростов, напоминающих по своему виду петушиные гребни или цветную капусту. Диагностика крупных кондилом затруднений не вызывает. Генитальные кондиломы локализуются в основном в местах мацерации: малые половые губы, влагалище, шейка матки, устье уретры, область ануса, кожные покровы. У мужчин ОК располагаются в области крайней плоти, на головке полового члена, перинатальной области, реже эндоуретально. Инкубационный период колеблется от одного до 12 месяцев (в среднем 3-6 месяцев).
Исследования последних десятилетий свидетельствуют о том, что 85% пациенток с типичным ОК вульвы и промежности имеют дополнительные очаги ПВЧ-инфекции во влагалище или шейке матки, и почти у каждой четвертой из них выявляются ассоциированные ПВЧ-инфекцией заболевания — цервикальные интраэпителиальные неоплазии (ЦВН) различной степени тяжести. Одной из клинических разновидностей заболеваний, вызываемых ПВЧ-инфекцией, являются боуэноидные папулы, связанные с ПЧ 16, иногда пигментированные на коже и слизистых оболочках представителей обоих полов, чаще напоминающие обычные бородавки или себорейный кератоз. В противоположность болезни Боуэна, боуэноидные папулы доброкачественные и спонтанно регрессируют, хотя изредка могут озлокачествляться. Течение бессимптомное.
Некоторые авторы к этой группе заболеваний относят верруциформную эпидермодисплазию Левандовского — Лютца. В основе этого заболевания лежат локальные и генетические нарушения, ассоциирующиеся с хронической ПВЧ-инфекцией.
J. M. Handley и W. J. Dinsmore (1994) на основании литературных данных, а также своих собственных исследований предложили классификацию клинических форм ПВЧ-инфекции и ассоциированных с ней заболеваний (табл.1).
В подавляющем большинстве случаев манифестные формы ПВЧ-инфекции сочетаются с другими заболеваниями, передающимися половым путем. По данным Бернарда К. и Муги К. (1996), манифестные формы ПВЧ-инфекции возникают, как правило, в результате действия ряда факторов:
- социальных;
- инфекционных, связанных с ассоциациями заболеваний, передающихся половым путем (ЗППП);
- связанных с изменением иммунного статуса.
Наиболее существенным является влияние ассоциированных с ПВЧ-поражениями инфекций урогенитального тракта: урогенитального хламидиоза, микоплазмоза, цитомегаловирусной и герпетической инфекции, дисбиотических состояний. Результатом их влияния на течение ПВЧ-инфекции является хронизация процесса, формирование стойких, как правило уже неспецифических воспалительных изменений со стороны мочеполовой сферы и значительные трудности в проведении терапевтических мероприятий.
Значимость наличия сопутствующей инфекции для лечения кондиломатоза объясняется следующими обстоятельствами.
- Наличие ЗППП, ассоциированных с ПВЧ-инфекцией, удлиняет срок лечения последних в среднем в три раза.
- В большинстве случаев рецидивы связаны с вышеуказанной причиной.
- Эпителизация эрозий шейки матки после разрушения кондилом может быть достигнута только при наличии предварительного сканирования по поводу сопутствующих ЗППП и бактериального вагиноза.
В течение многих лет обсуждалась возможность существования взаимосвязи между неоплазиями шейки матки с венерическими заболеваниями. В группе женщин, страдающих инвазивным раком шейки матки (РШМ), отмечена более высокая частота выявления неспецифической микрофлоры, включая трихомонадные и гарднереловые инфекции. Примеры такого влияния обсуждались в отношении Treponema pallidum, Neisseria gonorrhoeae, Chlamidia trachomatis, вируса простого герпеса типа 2, цитомегаловируса, вируса папилломы человека. Эпидемиологические исследования убедительно показали, что неоспоримым фактором риска возникновения предраковых изменений и рака шейки матки является генитальная ПВЧ-инфекция.
Принципы лечения ПВЧ-инфекции
Учитывая тот факт, что специфические противовирусные препараты и вакцины, действующие на ПВЧ, пока отсутствуют, принято считать, что полного устранения вируса из организма достичь невозможно. Задача терапии — устранение клинических и субклинических форм ВПЧ-инфекции.
На сегодняшний день в арсенале практикующих врачей имеется множество методов удаления аногенитальных бородавок. Эффективность их варьирует от 30 до 90%, но ни один из методов не является панацеей, так как частота рецидивов достаточно высока при любом способе лечения. Лечение должно быть строго индивидуальным: необходимо подбирать наиболее оптимальное решение в каждом конкретном случае, иногда учитывая пожелания самого пациента. Проблема рецидивов не зависит от выбора терапии. Рецидивы аногенитальных бородавок связаны чаще всего не с реинфекцией от полового партнера, а с реактивацией инфекции. Существуют три пути развития событий при отсутствии лечения:
- бородавки могут разрешаться самостоятельно;
- оставаться без изменений;
- прогрессировать.
При этом всегда нужно принимать во внимание возможность персистенции вируса при отсутствии каких-либо клинических проявлений.
Выбирая наиболее оптимальный в каждом конкретном случае метод, необходимо руководствоваться четырьмя основными характеристиками:
- эффективность при данной патологии;
- частота рецидивов после лечения;
- переносимость (минимум побочных эффектов);
- простота выполнения процедур.
Помимо удаления аногенитальных бородавок необходимо решать следующие немаловажные задачи:
1. Выявлять и лечить у больных с аногенитальными бородавками (и их половых партнеров) другие заболевания, передающиеся половым путем (ЗППП).
2. Проводить скрининг всех женщин с бородавками аногенитальной области на цервикальную внутриэпителиальную неоплазию (ЦВН) с применением цитологического исследования и кольпоскопии.
3. Поддерживать дальнейшее наблюдение за очагами ЦВН на ранних стадиях для своевременного выявления их прогрессирования или развития микроинвазивной карциномы.
4. Проводить активное лечение аногенитальных бородавок, неоплазий на ранних стадиях, протекающих с развернутой клинической картиной, неоплазий на поздних стадиях и плоскоклеточной карциномы.
5. Давать больным рекомендации по использованию презервативов и ограничению случайных половых контактов для предотвращения инфицирования (и реинфицирования) ВПЧ-инфекцией и другими ЗППП.
По сути, лечение аногенитальных ВПЧ-поражений направлено либо на разрушение папилломатозных очагов тем или иным методом, либо на стимуляцию противовирусного иммунного ответа, возможно сочетание этих подходов.
Деструктивные методы
Физические деструктивные методы
Хирургическое иссечение. В настоящее время применяется нечасто, в основном используется при лечении злокачественных новообразований, когда необходимо широкое иссечение. Данный метод может потребовать госпитализации в связи с тем, что при проведении иссечения может возникнуть достаточно сильное кровотечение, а длительный послеоперационный период потребует специальной терапии.
Электрохирургические методы. К ним относят электрокоагуляцию, электроакустику, фульгацию, электрохирургическое иссечение (электроэксцизия) с использованием электроножа. Не так давно в медицине стали использовать плазму. Нашими учеными был разработан оригинальный плазменный коагулятор (плазмаскин) ЭКХ-1, не имеющий зарубежных аналогов. Измерения температуры в плазме показали, что она может достигать 2000-2500°С. Такие высокие значения температуры, в свою очередь, обеспечивают возможность работать в бесконтактном режиме, существенно снижается время операции и тем самым уменьшается зона некроза. Кроме того, при таком воздействии в большинстве случаев не превышается болевой порог. Данный температурный режим обеспечивает практически полное сжигание новообразований.
Достоинства данного метода:
- доступность;
- дешевизна;
- достаточно высокая эффективность;
- возможность применения в амбулаторных условиях;
- снижена опасность кровотечений.
- необходимость обезболивания
- при использовании данного метода происходит выделение инфекционной ДНК ВПЧ вместе с образующимся дымом, поэтому необходимо создание адекватных условий для работы — вакуум-экстракция дыма, применение защитных масок.
Лазерное иссечение. Достаточно эффективным и безопасным методом является иссечение бородавок с помощью лазера. В практике применяют неодимовый и СО-лазеры. При использовании СО-лазера меньше повреждаются окружающие ткани, а неодимовый лазер дает лучший гемостатический эффект. Помимо того что лазер физически удаляет поражения, исследования показали, что лазерное излучение оказывает на ВПЧ токсическое действие. Для выполнения процедур требуется хорошо обученный персонал. При использовании лазеров необходимо обезболивание — чаще достаточно местной или локальной анестезии, что позволяет проводить процедуры в амбулаторных условиях. Лазерное иссечение и хирургические методы примерно одинаково эффективны. Лазеротерапию можно успешно применять для лечения распространенных, устойчивых к другой терапии кондилом. Она позволяет прекратить рецидивирование примерно у 40% больных. Исследования показали, что столь малоэффективный результат связан с тем, что СО-лазер неэффективен, когда речь идет об устранении генома из поражений, устойчивых к лечению (по данным метода ПЦР, молекулярно-биологическое излечение наступает у 26% больных).
Использование СО-лазера представляет собой метод выбора при лечении ЦВН. Применяют лазерную конизацию шейки матки. Рецидивы наблюдаются у 2% больных. Мягким методом лазеротерапии является вапоризация, не вызывающая практически никаких осложнений. Лазерная вапоризация успешно применяется при лечении ЦВН низкой степени. Рецидивы наблюдаются у 4% больных.
Лазеротерапия успешно используется для лечения остроконечных кандилом у беременных. Имеются сообщения о лечении беременных на 28–35-й неделе беременности. У большинства пациенток излечение наступало после первого сеанса. Каких-либо осложнений в родах или у новорожденных не выявлено.
Из побочных эффектов следует отметить изъязвление, кровотечение, вторичное инфицирование, рубцевание. Как и при использовании электрохирургических методов, происходит выделение ДНК ВПЧ с дымом, что также требует мер предосторожности.
Лазеротерапия не используется достаточно широко в связи с высокой стоимостью оборудования и необходимостью подготовки опытного персонала.
Криотерапия. Достаточно эффективный и безопасный метод, предполагающий использование в качестве хладагента жидкого азота, оксида азота и диоксида углерода. При этом происходит быстрое замораживание как внутри-, так и внеклеточной жидкости, приводящее к лизису и гибели клеток при оттаивании. Проведение криотерапии обычно не требует обезболивания, хотя при необходимости можно использовать местные анестетики. Криотерапию можно применять при лечении не очень больших бородавок различной локализации. Если же бородавки множественные, то удаление должно проводиться в несколько этапов. Для данного метода характерны следующие побочные явления: развитие местного покраснения, припухлости с последующим образованием пузырей и их изъязвлением. Для уменьшения повреждения окружающих тканей перед процедурой поверхность бородавок обрабатывают KY-гелем, который при замораживании дает возможность осторожно приподнять и отделить очаг поражения от подлежащего эпителия.
Метод может быть использован в гинекологической практике.
Чрезвычайно перспективным нам представляется сочетанное применение криодеструкции и плазменной коагуляции, позволяющее избежать недостатков, присущих вышеописанным методам в отдельности.
Химические деструктивные методы. Данная группа средств включает в себя растворы кислот, щелочей, солей. Среди них можно упомянуть ферезол, пероксид водорода, растворы акрихина и хингамина, препараты ртути и мышьяка, висмута, препараты на основе салициловой и молочной кислот, уксусную и азотную кислоты, соки туи и чистотела. Все эти средства легко доступны, однако обладают невысокой, плохо прогнозируемой эффективностью, дают многочисленные побочные эффекты.
Изопринозин следует применять в сочетании с местнодеструктивными методами лечения.
Эффективность комбинированного лечения ИП, по литературным данным, составляет от 38 до 96%.
Комбинированные методы лечения. Для лечения проявлений ПВЧ-инфекции предлагаются различные методики, основанные на использовании иммунных препаратов в сочетании с лазерным, электрохирургическим и криодеструктивным воздействием.
Сочетанное применение вышеуказанных методов позволяет уменьшить число рецидивов и тем самым повысить эффективность лечения.
Получены хорошие результаты при использовании комбинированного метода лечения кондилом, включающего разрушение очагов с помощью криодеструкции (температура воздействия от –160 до –180°С, экспозиция 40–120 с, двукратно) в сочетании со стимуляцией иммунитета. Для стимуляции местного иммунитета область поражения обрабатывали эмульсией, содержащей интерферон (ИФ), а для стимуляции иммунной системы всего организма назначали препарат кемантан по 0,2 г три раза в день внутрь в течение 10 дней.
Возможно сочетание различных деструктивных методов. При наличии проявлений ПВЧ-инфекции на коже и слизистых оболочках предварительно производят криораспыление в течение 10–30 с, позволяющее четко выявить границы поражения за счет характерной сосочковой поверхности поражений, которая при этом белеет. Затем область поражения подвергается воздействию плазмы (с помощью аппарата плазмаскин).
Ряд исследователей лучшим способом лечения аногенитальных бородавок признают хирургическое удаление всех видимых поражений с последующим местным введением ИФ. В некоторых случаях целесообразно общее и местное применение ИФ перед хирургическим иссечением обширных кондилом.
Терапевтический эффект от применения ИФ отсутствует, если заболевание длится более одного года, а также при иммунодефиците.
В настоящее время существует не так много средств, которые можно использовать после применения деструктивных методов. В частности, сейчас появился препарат импран для местного применения в области очагов поражения после деструктивного воздействия.
Специфическая противовирусная терапия
В настоящее время не существует препаратов, оказывающих специфическое действие на ВПЧ. Известные средства, подавляющие репликацию вируса простого герпеса (ацикловир, ганцикловир), оказались неэффективны при лечении аногенитальной ВПЧ-инфекции.
Теоретически вакцинация представляет собой идеальный метод лечения и профилактики аногенитальных бородавок.
Есть сообщения об эффективном применении индукторов ИФ. Представляет интерес местное применение низкомолекулярного производного имиквидахинолинамина — имиквимода, который является индуктором цитокинов и, в частности, Л-ИФ. Его используют в виде 5%-ного крема три раза в неделю либо ежедневно на ночь до полного исчезновения высыпаний (но не более 4 месяцев). Полное исчезновение кондилом наблюдается в 13–56% случаев. При ежедневном применении чаще развивались местные побочные эффекты: покраснение, отечность, эрозии. Крем особенно показан для лечения субклинической ВПЧ-инфекции. Возможно применение виразола.
Эффект от использования монотерапии ИФ все-таки недостаточно изучен и не очень высок, кроме того, необходимо принимать во внимание высокую стоимость такого лечения. В связи с этим данный метод не получил широкого распространения в практике.
Изопринозин. В последние годы пристальное внимание иммунологов привлек новый иммуномодулятор изопринозин, представляющий собой комплекс инозина и соли N,N-диметиламина-2-пропанола и Р-ацетаминобензойной кислоты. Препарат может применяться в виде таблеток либо раствора для парентерального инъецирования. Активным веществом в этом комплексе, по-видимому, является инозин, а соль аминоспирта стимулирует его проникновение через мембрану лимфоцитов и других клеток.
Изопринозин обладает мощным и широким иммуномодулирующим действием. Многочисленные данные и обширная литература свидетельствуют о том, что in vitro препарат существенно усиливает пролиферацию Т-лимфоцитов, индуцированную митогенами или специфическими антигенами, а также дифференцировку пре-Т-лимфоцитов в более зрелые Т-лимфоциты, сопровождающуюся появлением на их поверхности соответствующих антигенов. ИП также стимулирует индуцированную митогеном пролиферацию В-лимфоцитов. Доказано стимулирующее действие изопринолина на активность натуральных киллерных клеток (НК-клеток) у здоровых людей и функциональную способность цитотоксических Т-лимфоцитов. Препарат улучшает соотношение CD4+/CD8+; повышает выработку Т-лимфоцитами ИЛ-2; содействует созреванию и пролиферации Т-клеток; активизирует синтез ИЛ-1 макрофагами. ИП обладает противовирусным действием и препятствует использованию рибосомальной РНК для размножения вируса. Следует отметить, что в случае применения изопринолина с другими иммунокорректорами он существенно усиливал противовирусное действие последних.
Приняты различные схемы лечения с применением изопринолина в зависимости от размеров кондилом, их локализации и степени малигнизации.
Схема 1: лечение мелких, множественных остроконечных кандилом с низкой степенью малигнизации.
Препарат принимают по 2 табл. три раза в день в течение 14–28 дней.
Схема 2: лечение множественных кондилом с отдельными крупными кондиломами или плоской кондиломы шейки матки.
Среди применяемых в нашей стране и за рубежом химических препаратов, оказывающих деструктивное действие, можно выделить ТХУ и азотную кислоту, а также комбинированный кислотный препарат — солкодерм.
ТХУ и азотная кислота. ТХУ применяется в 80-90%-ной концентрации и вызывает образование локального коагуляционного некроза. Аналогичное действие оказывает раствор азотной кислоты. В силу своей дешевизны и доступности оба метода достаточно широко распространены и по сей день. Кислоты эффективны для лечения кондилом вульвы, препуциального мешка, венечной борозды, головки полового члена, особенно в тех случаях, когда противопоказано применение ПФ и ПФГ. Прижигания проводят один раз в неделю в течение 5-6 недель. Эффективность применения ТХУ и азотной кислоты составляет примерно 70-80%. В некоторых случаях может развиться местная реакция в виде мокнутия и изъязвления.
Солкодерм. Солкодерм — водный раствор, в качестве активной составляющей которого выступают продукты взаимодействия органических кислот (уксусной, щавелевой и молочной) и ионов металлов с азотной
кислотой. Раствор содержит нитриты в количестве 0,02 мг/мл.
Ниже перечислены свойства и механизм действия солкодерма, которые выделяют его среди других препаратов этой группы, использующихся в рамках деструктивных методов:
- при местном применении солкодерм вызывает немедленную прижизненную фиксацию ткани, на которую он наносится;
- действие препарата строго ограничивается местом применения;
- признаком немедленного эффекта является изменение окраски обрабатываемого участка;
- девитализированная ткань высыхает и темнеет (эффект мумификации);
- «мумифицированный» струп отторгается самостоятельно;
- процесс заживления непродолжителен, а осложнения (вторичная инфекция или рубцевание) редки.
Общая характеристика лечения солкодермом:
- препарат оказывает точно ограниченное местное действие на патологически измененную ткань, на которую он наносится, окружающая ткань при этом не повреждается;
- метод пригоден для лечения различных новообразований кожи;
- лечение безболезненно;
- быстрое заживление, отсутствие осложнений;
- лечение проводится амбулаторно и не требует специальной аппаратуры;
- отсутствие каких-либо ограничений для больного.
Показания к применению солкодерма: простые бородавки, подошвенные бородавки, аногенитальные бородавки (остроконечные кондиломы), себорейные кератозы, актинокератозы, базально-клеточные эпителиомы (базалиомы).
Солкодерм очень удобен в применении и достаточно эффективен для лечения кондилом любой локализации. В большинстве случаев достаточно однократного применения.
Цитотоксические препараты
Подофиллин (ПФ). Пофиллин — смола, полученная из растений P.pelatum и P.emodi, растущих в Северной Америке и Гималаях. Для лечения бородавок аногенитальной области применяют 10-25%-ный раствор ПФ в этаноле или настойке бензоина. Он связывается с аппаратом микротрубочек клетки и ингибирует митозы, а также подавляет транспорт нуклеиновых кислот, в результате чего происходит ингибирование синтеза ДНК и клеточного деления.
Применение ПФ является простым, доступным, достаточно безопасным методом лечения, который может быть использован в амбулаторных условиях, а также самостоятельно пациентами. Препарат наносят один-два раза в неделю в течение максимум 5 недель в количестве не более 0,5 мл за одну процедуру. Больному необходимо следить, чтобы вода не попадала на обработанное место в течение 4-6 часов после процедуры. ПФ не рекомендуется применять при вагинальных, цервикальных и внутриэпителиальных бородавках. По сведениям ряда авторов, частота рецидивирования варьирует от 0 до 67%.
Примерно у 10-15% больных развиваются местные побочные реакции в виде мокнущего контактного дерматита. Особенно тяжелые осложнения в виде множественных изъязвлений возникают при неправильном самостоятельном применении. В результате длительного или неправильного применения ПФ у больных могут возникать различные побочные реакции, такие как тошнота, рвота, боли в животе, диарея, симптомы поражения почек, миокарда, печени, ЦНС и костного мозга.
Применение ПФ противопоказано при беременности, т. к. были отмечены случаи тератогенного действия на плод и внутриутробной гибели плода.
Многие исследователи считают ПФ недостаточно изученным и грубоочищенным растительным экстрактом, в связи с чем рекомендуют использовать только высокоочищенные подофиллотоксины, причем самостоятельное применение препарата самими больными нежелательно в силу вышеуказанных осложнений.
Подофиллотоксин (ПФТ) (кондилин). ПФТ — наиболее активная в терапевтическом отношении фракция ПФ. Выпускается в виде растворов 0,25, 0,3 и 0,5%, а также в виде крема 0,15, 0,3 и 0,5%.
Обычно его назначают два раза в день в течение трех дней в неделю подряд на протяжении 4-5 недель.
Несмотря на то что ПФТ лучше очищен по сравнению с ПФ, сообщается о большой частоте побочных явлений при использовании ПФТ, особенно его 0,5%-ного раствора. Наиболее часто в результате применения ПФТ наблюдаются следующие побочные эффекты: местные воспалительные реакции (эритема, жжение, болезненность, зуд, мокнутие и эрозии в области аппликации). Хотя в литературе не описано системных побочных эффектов, рекомендуется ограничивать применение ПФТ дозой 0,2 мл за одну процедуру.
Недостатками ПФТ являются его высокая стоимость и большая длительность лечения.
5-фторурацил (5-ФУ). 5-фторурацил (5-ФУ) является антагонистом пиримидина и обладает способностью нарушать синтез как клеточной, так и вирусной ДНК. Для лечения бородавок аногенитальной области его назначают в виде 5%-ного крема. При лечении интравагинальных бородавок препарат назначается один раз на ночь в течение недели или один раз в неделю в течение 10 недель. Степень эффективности препарата, по мнению различных исследователей, составляет 85-90%. При применении 5-ФУ могут возникнуть мокнущие эрозии на слизистой влагалища, вплоть до развития тяжелого мокнущего контактного дерматита. При лечении бородавок терминальной части уретры крем вводится сразу после мочеиспускания на ночь в течение 3-8 дней. Полное излечение внутриуретральных бородавок наблюдается у 90-95% мужчин. Однако при лечении наблюдается множество побочных эффектов: стеноз и стриктуры уретры, дизурия, изъязвления. Препарат противопоказан при беременности.
Иммунологические методы
Интерферон. Поскольку вирус папилломы человека сохраняется в эпителиальных клетках и использование деструктивных методов не гарантирует от рецидивов, перспективным в этом плане является применение ИФ как в качестве монотерапии, так и в сочетании с другими методами лечения.
ИФ являются эндогенными цитокинами, обладающими противовирусными, антипролиферативными и иммуномодулирующими свойствами. Существуют три основных класса ИФ: лейкоцитарный (Л-ИФ), фибробластный (Ф-ИФ) и Т-лимфоцитарный (Т-ИФ). ИФ можно применять местно, внутриочагово и системно (подкожно, в/м или в/в). Установлено, что при использовании ИФ у пациентов в очагах поражения снижается количество вирусной ДНК (по данным ПЦР), что коррелирует с клиническим улучшением или исчезновением поражения.
Имеются данные, касающиеся использования для лечения кондилом отечественного ИФ — человеческого лейкоцитарного интерферона (ЧЛИ). Его применяли внутриочагово (под папиллому) в дозе 100 000-500 000 МЕ, на курс 3-6 процедур в сочетании с нанесением на поражения интерфероновой мази с активностью 40 МЕ. ЧЛИ можно назначать системно и при лечении распространенных поражений в сочетании с деструктивными методами.
Наиболее эффективным препаратом при различных способах, схемах и дозах введения можно считать Л-ИФ. При системном применении Л-ИФ полное исчезновение бородавок наблюдали у 11–100% пациентов. Эффективность применения Ф-ИФ составила 45–82%. Эффективность Т-ИФ, показанная в разных исследованиях, гораздо ниже, чем у Л-ИФ и Ф-ИФ, и варьирует от 7 до 57%.
Следует помнить, что бессистемное использование различных методов лечения приводит к высокому проценту рецидивов, однако разработка определенных алгоритмов, учитывающих пол больных, локализацию и количество высыпаний, позволяет существенно снизить количество рецидивов.
Таблица 1. Аногенитальная ВПЧ-инфекция и ассоциированные с ВПЧ заболевания
ВПЧ-инфекция
Развернутые клинические формы (видимые невооруженным глазом или не видимые, но определяющиеся при наличии соответствующей симптоматики):
- бородавки (остроконечные кондиломы, плоские кондиломы, вульгарные бородавки)
- симптоматические внутриэпителиальные неоплазии на ранних стадиях — койлоцитоз, дискератоз при отсутствии дисплазии (плоские кондиломы)
Субклинические формы (не видимые вооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом или гистологическом исследовании
- бессимптомные внутриэпителиальные неоплазии (ВН) на ранних стадиях — койлоцитоз, дискератоз при отсутствии дисплазии (плоские бородавки)
Латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ)
Источник

