Гистологическая оценка патологических изменений суставов при различных способах индукции хронического артрита у крыс
А.А. Мужикян(1), кандидат ветеринарных наук, руководитель лаборатории гистологии и патоморфологии, Е.В. Шекунова(1,2), кандидат биологических наук, руководитель группы экспериментальной фармакологии, В.А. Кашкин(1,2), кандидат медицинских наук, руководитель исследований, старший научный сотрудник, М.Н. Макарова1, доктор медицинских наук, заместитель директора, В.Г. Макаров(1), доктор медицинских наук, директор 1 -ЗАО «Институт экспериментальной фармакологии», 188663, Россия, Ленинградская обл., Всеволожский р-н, г.п. Кузьмоловский, ул. Заводская, д. 3, корп. 245; 2 — Институт фармакологии им. А.В. Вальдмана, Первый Санкт-Петебургский государственный медицинский университет им. И.П. Павлова, 197022, Санкт-Петербург, ул. Льва Толстого, д. 6-8 e-mail: muzhikyan.aa@doclinika.ru
Резюме
Цель данного исследования – апробация известных гистологических критериев оценки изменений в суставах и сравнительный анализ 2 экспериментальных моделей хронического артрита – артрита, индуцированного введением полного адъюванта Фрейнда, и артрита, вызванного введением каррагинина. Клинические и гистопатоморфологические признаки оценивались не только качественно, но и категориальной системе. Показано, что введение полного адьюванта Фрейнда моделирует состояние ревматоидного артрита. Напротив, введение каррагинина способствует развитию хронического воспалительного артрита, лишенного аутоиммунологического компонента. Полученные результаты могут служить основой для выбора определенного методического подхода для фармакологической оценки эффективности лекарственных препаратов с антиревматоидным, противовоспалительным и (или) иммуномодулирующими свойствами давления. Приводится информация об изменениях основных характеристик в зависимости от пола и возраста лабораторных животных. Каждая из рассмотренных линий грызунов имеет специфические свойства, характерные для сахарного диабета и метаболического синдрома, что позволяет всесторонне изучать механизмы развития патологий, а также потенциальных лекарственных препаратов для терапии данных заболеваний.
Введение
Ревматоидный артрит (РА) – хроническое системное заболевание соединительной ткани аутоиммунной природы, при котором поражаются суставы. РА страдают около 1% взрослого населения планеты [1] и около 1 млн населения Российской Федерации [2]. Заболевание распространено во всем мире, частота встречаемости увеличивается с возрастом, причем женщины болеют в 3 раза чаще, чем мужчины. Хотя причины возникновения РА окончательно неясны, хорошо изучены механизмы воспалительного процесса, который приводит к постепенному разрушению суставов [3]. Воспаление приводит к прогрессирующей деструкции хрящевой ткани суставов, синовиальной гиперплазии, синовиту, эрозии костной ткани, повышению уровня медиаторов воспаления.
В экспериментальных исследованиях хронический артрит моделируется введением различных агентов, в том числе введением полного адъюванта Фрейнда, лямбда-каррагинина, коллагена, формалина. Данные модели широко используются для изучения специфической противовоспалительной и противоревматоидной активности фармакологических веществ. Однако клиническая картина, развивающаяся при введении различных индуцирующих агентов, имеет свои особенности. Так, клинические признаки артрита появляются приблизительно через 10 дней после введения адъюванта и через 21 день после введения каррагинина [4]. Адъювант-индуцированный артрит (АИА) – это Т-лимфоцитарнозависимый артрит, который во многом схож с РА, включая развитие отека околосуставных тканей, деградацию хряща, потерю функциональной активности сустава, лимфоцитарную инфильтрацию внутрисуставной полости. При АИА наблюдается резорбция костной ткани, однако поражения хряща выражены в меньшей степени, чем при экспериментальном артрите, вызванном введением коллагена [5]. Напротив, каррагининовая модель артрита не сопровождается подобной активацией иммунного ответа, так как макрофаги не способны к переработке молекулы каррагинина, в результате чего происходит его накопление в лизосомах с развитием воспалительной реакции и последующей гибелью клетки [6]. Таким образом, активированные Т-клетки
не участвуют в запуске иммунного ответа при данной модели артрита.
В данном исследовании был проведен сравнительный анализ 2 экспериментальных моделей хронического артрита – артрита, индуцированного введением полного адъюванта Фрейнда, и артрита, вызванного введением каррагинина. Были детально изучены гистопатоморфологические изменения, которые наблюдались на разных этапах развития патологии. Полученные результаты могут служить основой для выбора определенного методического подхода для фармакологической оценки эффективности лекарственных препаратов с антиревматоидным, противовоспалительным и (или) иммуномодулирующими свойствами.
Материал и методы
Эксперименты выполнены на самках крыс линии Вистар массой 200–250 г (питомник «Рапполово», Россия). Животных содержали в стандартных условиях, согласно Директиве 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях и в соответствии с Санитарно-эпидемиологическими требованиями к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев) (СП 2.2.1.3218-17; утв. постановлением Главного государственного санитарного врача РФ № 41 от 29 августа 2014 г.).
В период адаптации крысы группами по 4 особей были размещены в прозрачных клетках из поликарбоната с площадью пола 1419 см 2 (минимально допустимая площадь на 1 животное – 250 см 2 ). В качестве подстила использовали древесные гранулы (ООО «Биосфера», Санкт-Петербург, Россия).
Корм для лабораторных животных «ЛБК–120», изготовленный в соответствии с ГОСТ Р 50258-92 «Комбикорма полнорационные для лабораторных животных», давали ad libitum в кормовое углубление стальной решетчатой крышки клетки.
Животные получали воду, очищенную и нормированную по органолептическим свойствам, по показателям рН, сухого остатка, восстанавливающих веществ, диоксида углерода, нитратов и нитритов, аммиака, хлоридов, сульфатов, кальция и тяжелых металлов на основании СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества». Воду в стандартных поилках со стальными крышками-носиками давали ad libitum.
Животных содержали в контролируемых условиях окружающей среды (при температуре 19–25°C и относительной влажности воздуха 30–70%, NH3≤10 мг/м 3 , CO2≤0,15 об.%). Световой режим составил 12 ч света и 12 ч темноты. Был установлен режим воздухообмена, обеспечивающий смену около 15 объемов помещения в час.
За неделю до начала эксперимента животные были рассажены в клетки индивидуального содержания.
Экспериментальные процедуры были одобрено комитетом по биоэтике НПО «Дом фармации» (БЭК №1.36/16) и выполнены в соответствии с рекомендациями Директивы 2010/63/EU Европейского парламента, Совета Европейского Союза от 22 сентября 2010 г. по охране животных и политикой Национальных институтов здоровья США «Принципы лабораторного ухода за животными». Все данные были собраны и проанализированы 2 независимыми наблюдателями, которые не знали о групповой принадлежности животных. Это исследование соответствовало принципам 3R (reduction, refinement and replacement). Все усилия были направлены на минимизацию страданий животных и сокращение их числа.
Индукция артрита и дизайн эксперимента. Адъювант-индуцированный артрит АИА. Для индукции артрита крысам в плантарную поверхность задней лапы вводили полный адъювант Фрейнда (complete Freund adjuvant (CFA)) производства Sigma-Aldrich в объеме 100 мкл [7, 8].
Каррагенин-индуцированный артрит (КИА). При моделировании каррагенин-индуцированного артрита в плантарную часть задней лапы крыс самок вводили 100 мкл 3% λ-каррагенина [9].
На 29-й день эксперимента животные были эвтаназированы в СО2-камере.
Гистологическое исследование. Исследуемые отделы конечностей ампутировали на уровне нижней трети голени рассечением мягких тканей, большой и малой берцовой костей, без нарушения целостности суставов, с фиксацией материала для гистологического исследования.
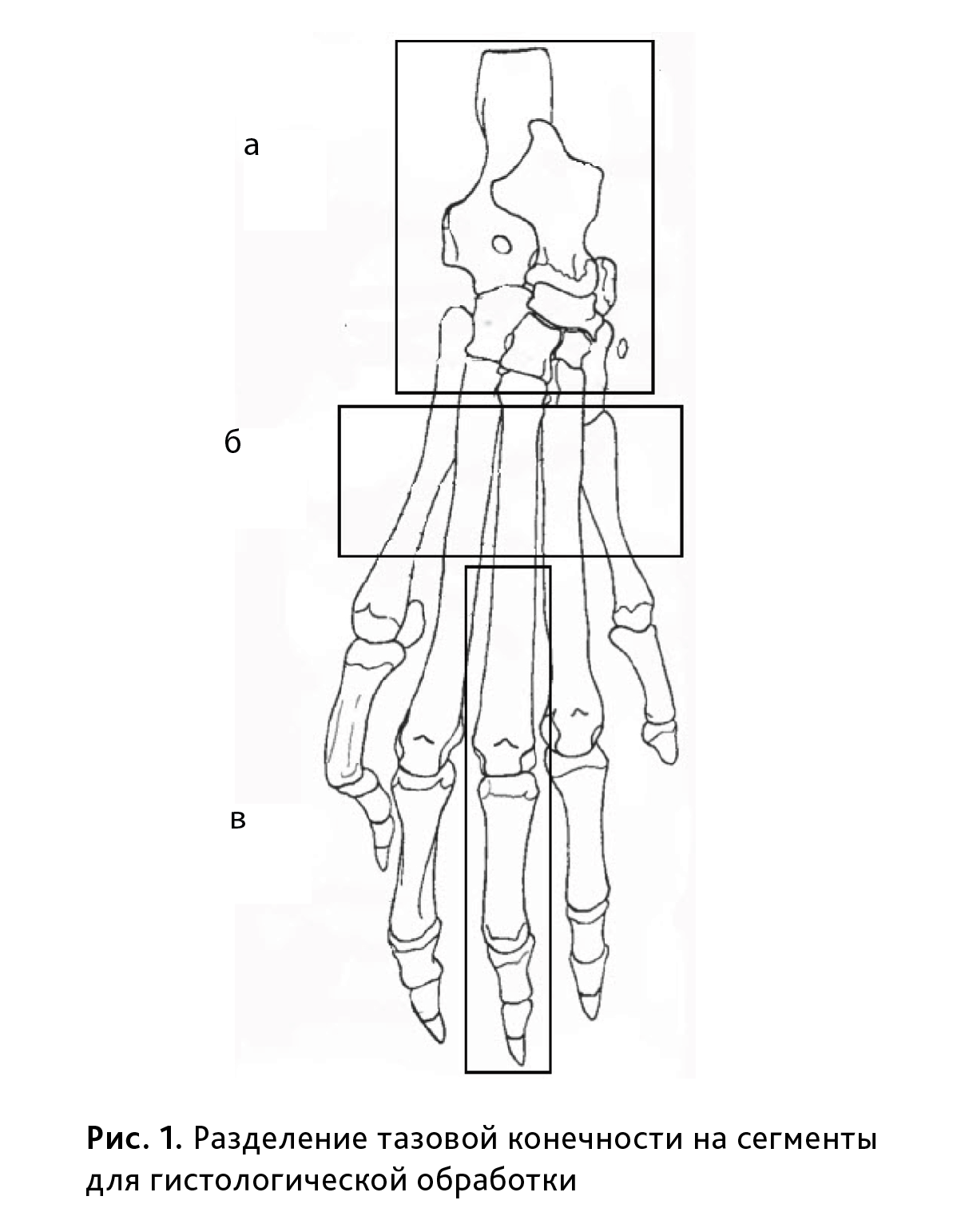
Гистологическому исследованию были подвергнуты пораженные суставы крыс, в том числе заплюсневый сустав, образованный блоком костей голени, костями заплюсны и проксимальным концом плюсневых костей, включающий в себя art. tarsocruralis, aa. intertarsae (представленный a. talocalcaneonavicularis, a. talocalcanea, a. calcaneocuboidea, a. cuneonavicularis), art. tarsometatarsea, а также плюснофаланговые, венечные и дистальные межфаланговые суставы пальцев стопы. Для этого конечности крыс фиксировали в 10% растворе нейтрального формалина, затем декальцинировали в электролитном растворе на основе муравьиной и соляной кислот в течение 14 дней, после чего делили на сегменты (рис. 1) и заливали в парафин. Затем изготавливали срезы толщиной 5–7 мкм, которые окрашивали гематоксилином и эозином.
Анализ гистологических препаратов выполняли с помощью светооптического микроскопа Carl Zeiss Axio Scope A1 (Германия) при увеличении 50, 100, 200 и 400. Микрофотографирование проводили цифровой фотокамерой AxioCam ICc 1 и с помощью программного обеспечения AxioVision Rel. 4.8 (Германия).
Структуры заплюсневого сустава и мягких тканей изучали на сагиттальных и плантарных срезах конечности (см. рис.1, а, б); для изучения межфаланговых суставов дистальную часть конечности отделяли поперечным разрезом плюсневых костей, а суставы, образованные плюсневыми костями, проксимальными, средними и дистальными фалангами изучали на сагиттальных срезах (см. рис. 1, в). Таким образом, было исследовано не менее 10 суставов каждого животного, попавших на срез. Критериями гистологической оценки служили изменения околосуставного аппарата (фиброзной и синовиальной капсулы), наличие воспалительного инфильтрата, состояние суставного хряща и костной ткани. В баллах от 0 (норма) – до 5 (максимальная выраженность патологии) оценивали 6 параметров.
Степень поражения суставов оценивали по модифицированной шкале Hegen (2003) [10], при этом анализировали следующие показатели:
- выраженность общего воспаления сустава (наличие инфильтрата, эдемы, выпота);
- степень сужения суставной полости;
- изменения костной ткани (остеолизис);
- изменения синовиальной оболочки (гиперплазия);
- выраженность паннуса (наличие в субинтимальном слое суставной капсулы грануляционной ткани с высоким содержанием фибробластов, лимфоцитов и макрофагов);
- степень дегенерации хряща.
При максимальной выраженности патологического процесса комплексная оценка для 1 животного составляла 30 баллов.
Более детально оценивали характер и выраженность изменений хрящевой ткани сустава по модифицированной шкале Mankin в баллах от 0 (норма) до 3 [11, 12]. Анализировали следующие показатели:
структура поверхности (1 балл – неровности, эрозии, 2 балла – трещины, 3 балла – расслоение);
клеточный состав (1 балл – незначительное снижение количества хондроцитов, 2 балла – значительное снижение количества хондроцитов, 3 балла – нет клеток);
окрашивание (1 балл – незначительное снижение окрашивания, 2 балла — значительное снижение окрашивания, 3 балла – нет окрашивания);
пролиферация клеток (1 балл – изогенные группы хондроцитов; по 2 клетки в группе; 2 балла – изогенные группы хондроцитов; по 2 и 3 клетки в группе); 3 балла – очаги пролиферации (более 3 клеток в группе).
При максимальной выраженности патологического процесса комплексная оценка для 1 животного составляла 12 баллов.
Статистическая обработка. Для анализа данных использовали тест Манна–Уитни, критерий Уилкокосона. Различия были определены при уровне значимости р
Источник
Болезни декоративных крыс
Крысы идеальны как домашние питомцы. Они ласковы, сообразительны, не требуют больших затрат по уходу, социально адаптированы. Однако даже хороший уход не гарантирует им жизнь без болезней. Часто наследственность оказывается сильнее и дает начало болезни декоративных крыс. Одомашненные крысы, не получающие должного ухода и лишенные сбалансированного питания, более уязвимы к факторам внешней среды, а, значит, болезненны.
Забота владельцев способствует качественно новому уровню жизни крыс. Постоянный доступ к еде, воде, соблюдение гигиены и наблюдение ветеринаром сохраняют здоровье и увеличивают продолжительность их жизни. В среднем декоративные крысы живут в 2–3 раза дольше диких, отличаются большей массой и плодовитостью.
Ожирение у крыс
В развитии почти любой болезни декоративных крыс, определенная роль принадлежит владельцу питомца . Недостаток знаний по уходу и кормлению, безответственность человека, способствуют, например, ожирению у крыс. Преобладание в пище высококалорийных белковых компонентов, тесная клетка без тренажеров, отсутствие прогулок по квартире — всё это делает питомца толстым и малоподвижным. У него появляются одышка и проблемы в работе сердца.
Лечение ожирения у крысы требует полного изменения рациона с включением овощей, фруктов и ничтожного количества белков. Помимо этого необходимо стимулирование физической активности питомца.
Пододерматит у крыс
Ожирение, в свою очередь, может послужить дополнительным фактором развития такой болезни декоративных крыс, как пододерматит. Воспаленные мокнущие раны и натоптыши на пятках причиняют животному боль. В природе когти крысы при ходьбе проникают в почву, а домашние питомцы этого лишены. В результате этого передняя часть лап приподнята вверх, и основная нагрузка приходится на пятки.
Плохая гигиена, лишний вес, влажный наполнитель препятствуют быстрому излечению. Первостепенные меры — стрижка когтей, коррекция питания для похудения, смена наполнителя на более мягкий, например, кукурузный.
Облысение у крыс
Бывает, что декоративная крыса начинает стремительно терять шерстяной покров. Облысение может произойти по разным причинам, одна из них — чрезмерный грумминг (выкусывание). Если крыса испытывает стресс, то может начать сама состригать зубами шерсть с лап. Стресс может быть вызван резкой сменой привычного интерьера или нахождением поблизости доминантного или агрессивного животного.
Другой причиной потери шерсти и появления расчесов являются паразиты — вши или клещи. Заразиться ими крысы могут от больных животным или через предметы ухода. Вшей можно увидеть невооруженным глазом или под лупой. Для обнаружения клещей ветеринарный врач берет соскоб с кожи. Для лечения используются противопаразитарные препараты, назначенные врачом ратологом. Хорошее состояние шерсти поддерживают витамины и минералы.
Опухоли у крыс
Некоторые факторы — пол, возраст, гормональный фон, генетика, экология и питание оказывают влияние на развитие у декоративных крыс доброкачественных и злокачественных опухолей. У самок крыс часто встречаются опухоли молочных желез и матки. У самцов декоративных крыс нередко обнаруживаются опухоли кожи или соединительной ткани. Можно столкнуться с такой опасной опухолью как лимфома. В настоящее время часто обнаруживаются опухоли головного мозга у крыс, для диагностики которых может потребоваться МРТ (магнитно-резонансная томография).
Для профилактики опухолевой болезни декоративных крыс рекомендуется регулярный осмотр у родентолога. Для самок крыс можно рассмотреть вопрос ранней стерилизации (овариогистерэктомии) — операции по удалению яичников и матки.
Болезни декоративных крыс — симптомы
Разные заболевания декоративной крысы начинаются с одинаковых симптомов. Так, чиханье у крыс может быть вызвано механическими раздражителями (мелкими частичками опилок, песка), аллергической реакцией на пахучие вещества, лекарственные препараты, компоненты корма, а также воспалительным процессом в верхних дыхательных путях. Инфекция верхних дыхательных путей может легко перейти в пневмонию и даже абсцессы легких у крыс. Поэтому важно быстрее начать диагностику, включая рентгенографию, для оценки тяжести процесса и выбора оптимального лечения. Оставленное без правильного лечения заболевание может закончиться смертью животного.
Домашние крысы чувствительны к болезням инфекционной этиологии, и они протекают у них крайне тяжело. Наиболее часто встречается микоплазмоз крыс. Микоплазма может поражать дыхательные пути, легкие, среднее ухо, приводить к воспалению матки у самок крыс.
Существуют также болезни крыс, заразные для человека. К ним относится дерматофития (лишай), лихорадка после укуса крыс, вызываемая Streptobacillus moniliformis. Во избежание этих болезней необходимо соблюдать меры личной безопасности и гигиены.
Источник